RD-02030 Spider Straps System for Spine Board
Product Information
The product is a full body restraint belt designed for use in
medical and clinical settings. It is intended to provide support
and restraint for patients during various medical procedures. The
belt is available in multiple models to accommodate different
patient sizes and needs.
Product Usage Instructions
1. Patient Selection: Before using the restraint belt, ensure
that it is suitable for the intended patient. Refer to the patient
selection criteria in the user manual to determine if the belt is
appropriate.
2. Application of the Belts: Follow these steps to correctly
apply the belts:
- Position the patient in a suitable position for the
procedure. - Place the belt around the patient’s body, ensuring a snug fit
without causing discomfort or restricting circulation. - Secure the belts according to the instructions provided,
ensuring they are properly fastened and adjusted.
3. Cleaning and Maintenance:
- Cleaning: Regularly clean the restraint belt using a mild
detergent and water. Avoid using harsh chemicals or abrasive
materials that may damage the belt. - Routine Maintenance: Perform routine maintenance tasks as
instructed in the user manual. This may include checking for any
signs of wear or damage and tightening any loose components. - Periodic Overhaul: Schedule periodic overhauls of the restraint
belt to ensure its continued functionality and safety. Follow the
recommended intervals provided in the manual. - Special Maintenance: In case of any specific maintenance
requirements or repairs, refer to the user manual or contact the
manufacturer for assistance.
4. Disposal: When the restraint belt reaches the end of its
lifespan or is no longer safe for use, dispose of it according to
local regulations and guidelines. Follow the instructions provided
in the user manual for proper disposal methods.
For any additional information or assistance, refer to the user
manual or contact the manufacturer.
Manuale d’uso e Manutenzione CINTURE DI TRATTENUTA INTEGRALE IT
Use and Maintenance Manual FULL BODY RESTRAINT BELT EN
Betriebs- und Wartungshandbuch INTEGRAL-HALTEGURTE DE
Manuel d’utilisation et d’entretien SANGLES ARAIGNÉES FR
Manual de uso y Mantenimiento CINTURONES DE SUJECIÓN/RETENCIÓN INTEGRAL
ES
Manual de Uso e Manutenção CINTOS DE RETENÇÃO INTEGRAL PT
EL
Manual de utilizare i întreinere CENTURI PENTRU IMOBILIZARE TOTAL RO
Návod k pouzití a údrzb CELOTLOVÉ FIXACNÍ POPRUHY CS
BG
Bruger- og vedligeholdelsesvejledning INTEGREREDE FASTSPÆNDINGSBÆLTER
DA
Käyttö- ja huolto-opas KOKOVARTALON KIINNITYSHIHNAT FI
Gebruikers- en onderhoudshandleiding INTEGRALE FIXATIEBANDEN NL
Bruks- og vedlikeholdsveiledning HELE SIKKERHETSBELTER NO
Instruktioner för drift och underhåll HELTÄCKANDE SÄKERHETSBÄLTEN SV
Uputstvo za upotrebu i odrzavanje INTEGRALNI SIGURNOSNI POJASEVI SR
Lietosanas un apkopes rokasgrmata INTEGRTAS DROSBAS JOSTAS LV
ZH
JA
SPENCER ITALIA SRL Via Provinciale n° 12 43038 Sala Baganza (PR) Italy
INDICE / CONTENTS / INHALTSVERZEICHNIS / SOMMAIRE
IT
1. MODELLI 2. DESTINAZIONE D’USO
8 8
2.1 DESTINAZIONE D’USO E BENEFICI CLINICI
8
2.2 PAZIENTI DESTINATARI
8
2.3 CRITERI DI SELEZIONE PAZIENTI
8
2.4 CONTROINDICAZIONI ED EFFETTI COLLATERALI
INDESIDERATI
8
2.5 UTILIZZATORI E INSTALLATORI
8
2.5.1 FORMAZIONE UTILIZZATORI
8
2.5.2 FORMAZIONE INSTALLATORE
8
3. STANDARD DI RIFERIMENTO
8
4. INTRODUZIONE
8
4.1 UTILIZZO DEL MANUALE
8
4.2 ETICHETTATURA E CONTROLLO TRACCIABILITÀ
DEL DISPOSITIVO
8
4.3 SIMBOLI
9
4.4 GARANZIA E ASSISTENZA
9
5. AVVERTENZE/PERICOLI
9
6. AVVERTENZE SPECIFICHE
10
7. RISCHIO RESIDUO
10
8. DATI TECNICI E COMPONENTI
10
9. MESSA IN FUNZIONE
10
10. CARATTERISTICHE FUNZIONALI
11
11. MODALITA’ D’USO
11
11.1 APPLICAZIONE DELLE CINTURE
11
12. PULIZIA E MANUTENZIONE
11
12.1 PULIZIA
11
12.2 MANUTENZIONE ORDINARIA
11
12.3 REVISIONE PERIODICA
11
12.4 MANUTENZIONE STRAORDINARIA
12
12.5 TEMPO DI VITA
12
13. TABELLA GESTIONE GUASTI
12
14. ACCESSORI
12
15. RICAMBI
12
16. SMALTIMENTO
12
EN
1. MODELS
13
2. INTENDED USE
13
2.1 INTENDED USE AND CLINICAL BENEFITS
13
2.2 TARGET PATIENTS
13
2.3 PATIENT SELECTION CRITERIA
13
2.4 CONTRAINDICATIONS AND UNWANTED SIDE
EFFECTS
13
2.5 USERS AND INSTALLERS
13
2.5.1 USER TRAINING
13
2.5.2 INSTALLER TRAINING
13
3. REFERENCE STANDARDS
13
4. INTRODUCTION
13
4.1 USING THE MANUAL
13
4.2 DEVICE LABELLING AND TRACEABILITY
13
4.3 SYMBOLS
14
4.4 WARRANTY AND SERVICE
14
5. WARNINGS/DANGERS
14
6. SPECIFIC WARNINGS
15
7. RESIDUAL RISK
15
8. TECHNICAL DATA AND COMPONENTS
15
9. COMMISSIONING
15
10. OPERATING CHARACTERISTICS
15
11. PROPER USE
16
11.1 APPLYING THE BELTS
16
12. CLEANING AND MAINTENANCE
16
12.1 CLEANING
16
12.2 ROUTINE MAINTENANCE
16
12.3 PERIODIC OVERHAUL
16
12.4 SPECIAL MAINTENANCE
16
12.5 LIFE SPAN
17
13. TROUBLESHOOTING TABLE
17
2
14. ACCESSORIES
17
15. SPARE PARTS
17
16. DISPOSAL
17
1. MODELLE
18
DE 2. VERWENDUNGSZWECK
18
2.1 VERWENDUNGSZWECK UND KLINISCHER
NUTZEN
18
2.2 ZIELPATIENTEN
18
2.3 AUSWAHLKRITERIEN FÜR PATIENTEN
18
2.4 GEGENANZEIGEN UND UNERWÜNSCHTE
NEBENWIRKUNGEN
18
2.5 ANWENDER UND TECHNIKER
18
2.5.1 ANWENDERAUSBILDUNG
18
2.5.2 AUSBILDUNG INSTALLATEUR
18
3. BEZUGSRICHTLINIEN
18
4. EINLEITUNG
18
4.1 GEBRAUCH DES HANDBUCHS
18
4.2 TYPENSCHILDER UND RÜCKVERFOLGBARKEIT
DES PRODUKTS
18
5. WARNUNGEN/GEFAHREN
19
6. SPEZIFISCHE HINWEISE
20
7. RESTRISIKO
20
8. TECHNISCHE DATEN UND KOMPONENTEN
20
9. INBETRIEBNAHME
20
10. ANWENDUNGSEIGENSCHAFTEN
21
11. GEBRAUCHSWEISE
21
11.1 ANWENDUNG DER GURTE
21
12. REINIGUNG UND WARTUNG
21
12.1 REINIGUNG
21
12.2 ORDENTLICHE WARTUNG
21
12.3 REGELMÄSSIGE REVISION
22
12.4 AUSSERORDENTLICHE WARTUNG
22
12.5 LEBENSDAUER
22
13. SCHADENSTABELLE
22
14. ZUBEHÖR
22
15. ERSATZTEILE
22
16. ENTSORGUNG
22
FR
1. MODÈLES 2. UTILISATION
23 23
2.1 UTILISATION ET BÉNÉFICES CLINIQUES
23
2.2 PATIENTS DESTINATAIRES
23
2.3 CRITÈRES DE SÉLECTION DES PATIENTS
23
2.4 CONTRE-INDICATIONS ET EFFETS
COLLATÉRAUX INDÉSIRABLES
23
2.5 UTILISATEURS ET INSTALLATEURS
23
2.5.1 FORMATION DES UTILISATEURS
23
2.5.2 FORMATION INSTALLATEUR
23
3. STANDARD DE RÉFÉRENCE
23
4. INTRODUCTION
23
4.1 UTILISATION DU MANUEL
23
4.2 ÉTIQUETAGE ET CONTRÔLE DE LA
TRAÇABILITÉ DU DISPOSITIF
23
5. AVERTISSEMENTS/DANGERS
24
6. AVERTISSEMENTS SPÉCIFIQUES
25
7. RISQUE RÉSIDUEL
25
8. DONNÉES TECHNIQUES ET COMPOSANTS
25
9. MISE EN SERVICE
25
10. CARACTÉRISTIQUES FONCTIONNELLES
26
11. MODALITÉS D’UTILISATION
26
11.1 APPLICATION DES SANGLES
26
12. NETTOYAGE ET ENTRETIEN
26
12.1 NETTOYAGE
26
12.2 ENTRETIEN ORDINAIRE
26
12.3 RÉVISION PÉRIODIQUE
27
ÍNDICE / ÍNDICE /
12.4 ENTRETIEN EXTRAORDINAIRE
27
12.5 DURÉE DE VIE
27
13. TABLEAU DE GESTION DES PANNES
27
14. ACCESSOIRES
27
15. PIÈCES DÉTACHÉES
27
16. ÉLIMINATION
27
ES 1. MODELOS 2. DESTINO DE USO
28 28
2.1 DESTINO DE USO Y BENEFICIOS CLÍNICOS 28
2.2 PACIENTES DESTINATARIOS
28
2.3 CRITERIOS DE SELECCIÓN DE LOS PACIENTES 28
2.4 CONTRAINDICACIONES Y EFECTOS
COLATERALES NO DESEADOS
28
2.5 USUARIOS Y ENCARGADOS DE SU
COLOCACIÓN
28
2.5.1 FORMACIÓN DE LOS USUARIOS
28
2.5.2 FORMACIÓN DEL INSTALADOR
28
3. NORMAS DE REFERENCIA
28
4. INTRODUCCIÓN
28
4.1 USO DEL MANUAL
28
4.2 ETIQUETADO Y CONTROL DE SEGUIMIENTO
DEL DISPOSITIVO
28
4.3 SÍMBOLOS
29
4.4 GARANTÍA Y ASISTENCIA
29
5. ADVERTENCIAS/PELIGROS
29
6. ADVERTENCIAS ESPECÍFICAS
30
7. RIESGO RESIDUAL
30
8. DATOS TÉCNICOS Y COMPONENTES
30
9. PUESTA EN FUNCIONAMIENTO
30
10. CARACTERÍSTICAS DE FUNCIONAMIENTO
31
11. MODO DE USO
31
11.1 APLICACIONES DE LOS CINTURONES
31
12. LIMPIEZA Y MANTENIMIENTO
31
12.1 LIMPIEZA
31
12.2 MANTENIMIENTO ORDINARIO
31
12.3 REVISIÓN PERIÓDICA
32
12.4 MANTENIMIENTO EXTRAORDINARIO
32
12.5 TIEMPO DE VIDA ÚTIL
32
13. TABLA DE GESTIÓN DE FALLAS
32
14. ACCESORIOS
32
15. RECAMBIOS
32
16. ELIMINACIÓN
32
1. MODELOS
33
PT 2. USO PRETENDIDO
33
2.1 USO PRETENDIDO E BENEFÍCIOS CLÍNICOS 33
2.2 PACIENTES DESTINATÁRIOS
33
2.3 CRITÉRIOS DE SELEÇÃO DOS PACIENTES
33
2.4 CONTRAINDICAÇÕES E EFEITOS COLATERAIS
INDESEJADOS
33
2.5 UTILIZADORES E INSTALADORES
33
2.5.1 FORMAÇÃO DOS UTILIZADORES
33
2.5.2 FORMAÇÃO DO INSTALADOR
33
3. NORMATIVA DE REFERÊNCIA
33
4. INTRODUÇÃO
33
4.1 UTILIZAÇÃO DO MANUAL
33
4.2 ETIQUETAGEM E CONTROLO DA
RASTREABILIDADE DO PRODUTO
33
4.3 SÍMBOLOS
34
4.4 GARANTIA E ASSISTÊNCIA
34
5. ADVERTÊNCIAS/PERIGOS
34
6. ADVERTÊNCIAS ESPECÍFICAS
35
7. RISCO RESIDUAL
35
8. DADOS TÉCNICOS E COMPONENTES
35
9. COLOCAÇÃO EM FUNÇÃO
35
10. CARACTERÍSTICAS FUNCIONAIS
35
11. MODO DE UTILIZAÇÃO
36
11.1 APLICAÇÃO DOS CINTOS
36
12. LIMPEZA E MANUTENÇÃO
36
12.1 LIMPEZA
36
12.2 MANUTENÇÃO ORDINÁRIA
36
12.3 REVISÃO PERIÓDICA
36
12.4 MANUTENÇÃO EXTRAORDINÁRIA
36
12.5 VIDA ÚTIL
37
13. TABELA PARA A RESOLUÇÃO DE PROBLEMAS 37
14. ACESSÓRIOS
37
15. PEÇAS SOBRESSALENTES
37
16. ELIMINAÇÃO
37
EL
1. 2.
38 38
2.1 38
2.2
38
2.3
38
2.4
38
2.5
38
2.5.1
38
2.5.2
38
3.
38
4.
38
4.1
38
4.2
38
4.3
39
4.4
39
5. /
39
6.
40
7.
40
8.
40
9.
41
10.
41
11.
41
11.1
41
12.
41
12.1
42
12.2
42
12.3
42
12.4
42
12.5
42
13.
42
14.
42
15.
42
16.
42
3
INDEX / INDEX / / INDHOLDSFORTEGNELSE
RO
1. MODELE
43
2. DOMENIUL DE UTILIZARE
43
2.1 DOMENIUL DE UTILIZARE I
BENEFICIILE CLINICE
43
2.2 PACIENII DESTINATARI
43
2.3 CRITERII DE SELECTARE A PACIENILOR
43
2.4 CONTRAINDICAII I EFECTE SECUNDARE
NEDORITE
43
2.5 UTILIZATORI I INSTALATORI
43
2.5.1 FORMAREA UTILIZATORILOR
43
2.5.2 FORMAREA INSTALATORULUI
43
3. STANDARD DE REFERIN
43
4. INTRODUCERE
43
4.1 UTILIZAREA MANUALULUI
43
4.2 ETICHETAREA I CONTROLUL TRASABILITII
DISPOZITIVULUI
43
4.3 SIMBOLURI
44
4.4 GARANIE I ASISTEN
44
5. AVERTISMENTE/PERICOLE
44
6. AVERTISMENTE SPECIFICE
45
7. RISC REZIDUAL
45
8. DATE TEHNICE I COMPONENTE
45
9. UTILIZAREA
45
10. CARACTERISTICI FUNCIONALE
46
11. MOD DE UTILIZARE
46
11.1 APLICAREA CENTURILOR
46
12. CURAREA I ÎNTREINEREA
46
12.1 CURAREA
46
12.2 ÎNTREINEREA OBINUIT
46
12.3 REVIZIA PERIODIC
46
12.4 ÎNTREINEREA SPECIAL
47
12.5 DURATA DE VIA
47
13. TABEL DE GESTIONARE A DEFECIUNILOR
47
14. ACCESORII
47
15. PIESE DE SCHIMB
47
16. ELIMINAREA
47
CS
1. MODELY 2. URCENÝ ÚCEL
48 48
2.1 URCENÝ ÚCEL A KLINICKÝ PÍNOS
48
2.2 CÍLOVÉ SKUPINY PACIENT
48
2.3 KRITÉRIA VÝBRU PACIENT
48
2.4 KONTRAINDIKACE A NEZÁDOUCÍ VEDLEJSÍ
ÚCINKY
48
2.5 UZIVATELÉ A OSOBY ODPOVDNÉ ZA
INSTALACI
48
2.5.1 ODBORNÁ PÍPRAVA UZIVATEL
48
2.5.2 ODBORNÁ PÍPRAVA OSOBY
ODPOVDNÉ ZA INSTALACI
48
3. POUZITÉ NORMY
48
4. ÚVOD
48
4.1 POUZITÍ NÁVODU
48
4.2 OZNACOVÁNÍ A KONTROLA
VYSLEDOVATELNOSTI PROSTEDKU
48
4.4 ZÁRUKA A SERVIS
49
5. VAROVÁNÍ/NEBEZPECÍ
49
6. SPECIFICKÁ VAROVÁNÍ
50
7. ZBYTKOVÉ RIZIKO
50
8. TECHNICKÉ ÚDAJE A SOUCÁSTI
50
9. PRVNÍ POUZITÍ
50
10. FUNKCNÍ CHARAKTERISTIKY
51
11. ZPSOB POUZITÍ
51
11.1 NASAZENÍ POPRUH
51
12. CISTNÍ A ÚDRZBA
51
12.1 CISTNÍ
51
12.2 ÁDNÁ ÚDRZBA
51
12.3 PRAVIDELNÁ PROVRKA
51
12.4 MIMOÁDNÁ ÚDRZBA
52
12.5 ZIVOTNOST
52
13. TABULKA PORUCH
52
14. PÍSLUSENSTVÍ
52
15. NÁHRADNÍ DÍLY
52
16. LIKVIDACE
52
BG
1.
53
2.
53
2.1 53
2.2 ,
53
2.3
53
2.4
53
2.5
53
2.5.1
53
2.5.2
53
3.
53
4.
53
4.1
53
4.2
53
4.3
54
4.4
54
5. /
54
6.
55
7.
55
8.
55
9.
55
10.
56
11.
56
11.1
56
12.
56
12.1
56
12.2
56
12.3
57
12.4
57
12.5
57
13.
57
14.
57
15.
57
16.
57
DA
1. MODELLER
58
2. ANVENDELSESFORMÅL
58
2.1 PÅTÆNKT ANVENDELSE OG KLINISKE
FORDELE
58
2.2 MODTAGERPATIENTER
58
2.3 UDVÆLGELSESKRITERIER FOR PATIENTER 58
2.4 KONTRAINDIKATIONER OG BIVIRKNINGER 58
2.5 BRUGERE OG INSTALLATØRER
58
2.5.1 BRUGERTRÆNING
58
2.5.2 UDDANNELSE AF INSTALLATØR
58
3. REFERENCESTANDARD
58
4. INDLEDNING
58
4.1 BRUG AF DENNE VEJLEDNING
58
4.2 ENHEDENS MÆRKNING OG SPORBARHED 58
4.3 SYMBOLER
59
4.4 GARANTI OG TEKNISK ASSISTANCE
59
5. ADVARSLER/FARER
59
6. SPECIFIKKE ADVARSLER
60
7. RESTERENDE RISIKO
60
8. TEKNISKE DATA OG KOMPONENTER
60
9. IDRIFTSÆTTELSE
60
4
HAKEMISTO / INHOUDSOPGAVE / INNHOLDSFORTEGNELSE
10. FUNKTIONELLE EGENSKABER
61
11. ANVENDELSE
61
11.1 ANVENDELSE AF BÆLTERNE
61
12. RENGØRING OG VEDLIGEHOLDELS
61
12.1 RENGØRING
61
12.2 RUTINEMÆSSIG VEDLIGEHOLDELSE
61
12.3 PERIODISK GENNEMGANG
61
12.4 EKSTRAORDINÆR VEDLIGEHOLDELSE
62
12.5 LEVETID
62
13. FEJLFINDING
62
14. TILBEHØR
62
15. RESERVEDELE
62
16. BORTSKAFFELSE
62
FI 1. MALLIT 2. KÄYTTÖTARKOITUS
63 63
2.1 KÄYTTÖTARKOITUS JA KLIINISET HYÖDYT 63
2.2 KOHDEPOTILAAT
63
2.3 POTILAIDEN VALINTAKRITEERIT
63
2.4 KONTRAINDIKAATIOT JA EI-TOIVOTUT
SIVUVAIKUTUKSET
63
2.5 KÄYTTÄJÄT JA ASENTAJAT
63
2.5.1 KÄYTTÄJIEN KOULUTUS
63
2.5.2 ASENTAJAN KOULUTUS
63
3. VIITEDIREKTIIVI
63
4. JOHDANTO
63
4.1 OPPAAN KÄYTTÖ
63
4.2 ETIKETÖINTI JA LAITTEEN JÄLJITETTÄVYYDEN
TARKASTUS
63
4.3 SYMBOLIT
64
4.4 TAKUU JA HUOLTO
64
5. VAROITUKSET/VAARAT
64
6. ERITYISET VAROITUKSET
65
7. JÄÄNNÖSRISKI
65
8. TEKNISET TIEDOT JA KOMPONENTIT
65
9. KÄYTTÖÖNOTTO
65
10. TOIMINNALLISET OMINAISUUDET
66
11. KÄYTTÖTAPA
66
11.1 HIHNOJEN KÄYTTÖ
66
12. PUHDISTUS JA HUOLTO
66
12.1 PUHDISTUS
66
12.2 MÄÄRÄAIKAISHUOLTO
66
12.3 SÄÄNNÖLLINEN TARKASTUS
66
12.4 YLIMÄÄRÄINEN HUOLTO
67
12.5 KÄYTTÖIKÄ
67
13. VIANMÄÄRITYSTAULUKKO
67
14. LISÄVARUSTEET
67
15. VARAOSAT
67
16. HÄVITTÄMINEN
67
NL 1. MODELLEN 2. GEBRUIKSBESTEMMING
68 68
2.1 GEBRUIKSBESTEMMING EN KLINISCHE
VOORDELEN
68
2.2 DOELGROEP PATIËNTEN
68
2.3 KEUZECRITERIA PATIËNTEN
68
2.4 CONTRA-INDICATIES EN ONGEWENSTE
BIJWERKINGEN
68
2.5 GEBRUIKERS EN INSTALLATEURS
68
2.5.1 TRAINING VAN DE GEBRUIKERS
68
2.5.2 TRAINING VAN DE INSTALLATEUR
68
3. REFERENTIENORM
68
4. INLEIDING
68
4.1 GEBRUIK VAN DE HANDLEIDING
68
4.2 ETIKETTERING EN
TRACEERBAARHEIDSCONTROLE VAN
HET HULPMIDDEL
68
4.3 SYMBOLEN
69
4.4 GARANTIE EN ASSISTENTIE
69
5. WAARSCHUWINGEN/GEVAREN
69
6. SPECIFIEKE WAARSCHUWINGEN
70
7. RESTRISICO
70
8. TECHNISCHE GEGEVENS EN COMPONENTEN
70
9. INGEBRUIKNAME
70
10. FUNCTIONELE EIGENSCHAPPEN
71
11. GEBRUIK
71
11.1 BANDTOEPASSING
71
12. REINIGING EN ONDERHOUD
71
12.1 REINIGING
71
12.2 ROUTINEONDERHOUD
71
12.3 PERIODIEKE REVISIE
72
12.4 BUITENGEWOON ONDERHOUD
72
12.5 LEVENSDUUR
72
13. TABEL BEHEER DEFECTEN
72
14. ACCESSOIRES
72
15. ONDERDELEN
72
16. VERWIJDERING
72
1. MODELLER
73
NO 2. BRUKSFORMÅL
73
2.1 BRUKSFORMÅL OG KLINISKE FORDELER
73
2.2 PASIENTBRUKERE
73
2.3 KRITERIER FOR VALG AV PASIENTER
73
2.4 KONTRAINDIKASJONER OG UØNSKEDE
BIVIRKNINGER
73
2.5 BRUKERE OG INSTALLATØRER
73
2.5.1 OPPLÆRING AV BRUKERE
73
2.5.2 OPPLÆRING AV INSTALLATØR
73
3. REFERANSESTANDARD
73
4. INTRODUKSJON
73
4.1 BRUK AV VEILEDNINGEN
73
4.2 MERKING OG KONTROLL OG SPORING
AV INNRETNINGEN
73
4.3 SYMBOLER
74
4.4 GARANTI OG ASSISTANSE
74
5. ADVARSLER/FARER
74
6. SPESIFIKKE ADVARSLER
75
7. RESTRISIKO
75
8. TEKNISKE DATA OG KOMPONENTER
75
9. SETTE I FUNKSJON
75
10. FUNKSJONSEGENSKAPER
76
11. BRUKSMÅTE
76
11.1 PÅFØRING AV BELTENE
76
12. RENGJØRING OG VEDLIKEHOLD
76
12.1 RENGJØRING
76
12.2 ORINDÆRT VEDLIKEHOLD
76
12.3 REGELMESSIG REVISJON
76
12.4 EKSTRAORDINÆRT VEDLIKEHOLD
77
12.5 LEVETID
77
13. FEILSØKINGSTABELL
77
14. TILBEHØR
77
15. RESERVEDELER
77
16. KASSERING
77
5
INNEHÅLL / SADRZAJ / INDEKSS
SV
1. MODELLER 2. ANVÄNDNINGSOMRÅDE
78 78
2.1 AVSEDD ANVÄNDNING OCH
KLINISKA FÖRDELAR
78
2.2 ANVÄNDANDE PATIENTGRUPP
78
2.3 PATIENTURVALSKRITERIER
78
2.4 KONTRAINDIKATIONER OCH OÖNSKADE
BIVERKNINGAR
78
2.5 ANVÄNDARE OCH INSTALLATÖRER
78
2.5.1 ANVÄNDARUTBILDNING
78
2.5.2 INSTALLATÖRSUTBILDNING
78
3. REFERENSSTANDARDER
78
4. INLEDNING
78
4.1 ANVÄNDNING AV HANDBOKEN
78
4.2 ENHETSMÄRKNING OCH
SPÅRBARHETSKONTROLL
78
4.3 SYMBOLER
79
4.4 GARANTI OCH ASSISTANS
79
5. VARNINGAR/ FAROR
79
6. SÄRSKILDA VARNINGAR
80
7. KVARVARANDE RISKER
80
8. TEKNISKADATA OCH KOMPONENTER
80
9. IDRIFTTAGNING
80
10. FUNKTIONSEGENSKAPER
81
11. ANVÄNDNINGSSÄTT
81
11.1 PÅSÄTTNING AV BÄLTEN
81
12. RENGÖRING OCH UNDERHÅLL
81
12.1 RENGÖRING
81
12.2 ODINARIE UNDERHÅLL
81
12.3 PERIODISK ÖVERSYN
81
12.4 SÄRSKILT UNDERHÅLL
82
12.5 LIVSLÄNGD
82
13. FELHANTERINGSTABELL
82
14. TILLBEHÖR
82
15. RESERVDELAR
82
16. KASSERING
82
1. MODELI
83
SR 2. NAMENA
83
2.1 NAMERAVANA UPOTREBA I KLINICKE
PREDNOSTI
83
2.2 PACIJENITI KOJIMA SU NAMENJENE
83
2.3 KRITERIJUMI ZA ODABIR PACIJENATA
83
2.4 KONTRAINDIKACIJE I NEZELJENE NUSPOJAVE 83
2.5 KORISNICI I INSTALATERI
83
2.5.1 OBUKA KORISNIKA
83
2.5.2 OBUKA INSTALATERA
83
3. REFERENTNI STANDARD
83
4. UVOD
83
4.1 UPOTREBA UPUTSTVA
83
4.2 OZNACAVANJE UREAJA I KONTROLA
SLEDLJIVOSTI
83
4.3 SIMBOLI
84
4.4 GARANCIJA I SERVIS
84
5. UPOZORENJA/OPASNOSTI
84
6. POSEBNA UPOZORENJA
85
7. PREOSTALI RIZICI
85
8. TEHNICKI PODACI I KOMPONENTE
85
9. STAVLJANJE U UPOTREBU
85
10. RADNE KARAKTERISTIKE
85
11. NACIN UPOTREBE
86
11.1 PRIMENA POJASEVA
86
12. CISENJE I ODRZAVANJE
86
12.1 CISENJE
86
12.2 REDOVNO ODRZAVANJE
86
12.3 PERIODICNI PREGLED
86
12.4 VANREDNO ODRZAVANJE
86
12.5 ZIVOTNI VEK
86
13. TABELA UPRAVLJANJA KVAROVIMA
87
14. DODATNI PRIBOR
87
15. REZERVNI DELOVI
87
16. ODLAGANJE
87
LV
1. MODEI 2. PAREDZTAIS LIETOJUMS
88 88
2.1 PAREDZTAIS LIETOJUMS UN KLNISKIE
IEGUVUMI
88
2.2 MERA PACIENTI
88
2.3 PACIENTU IZVLES KRITRIJI
88
2.4 KONTRINDIKCIJAS UN BLAKUSPARDBAS 88
2.5 LIETOTJI UN UZSTDTJI
88
2.5.1 LIETOTJU APMCBA
88
2.5.2 UZSTDTJU APMCBA
88
3. ATSAUCES STANDARTS
88
4. IEVADS
88
4.1 ROKASGRMATAS IZMANTOSANA
88
4.2 IERCES MARJUMI UN IZSEKOJAMBAS
KONTROLE
88
4.3 SIMBOLI
89
4.4 GARANTIJA UN ATBALSTS
89
5. BRDINJUMI/APDRAUDJUMI
89
6. PASI BRDINJUMI
90
7. ATLIKUSAIS RISKS
90
8. TEHNISKIE DATI UN SASTVDAAS
90
9. NODOSANA EKSPLUATCIJ
90
10. FUNKCIONLS PASBAS
90
11. LIETOSANAS INSTRUKCIJA
91
11.1 JOSTU LIETOJUMS
91
12. TRSANA UN APKOPE
91
12.1 TRSANA
91
12.2 KRTJ APKOPE
91
12.3 PERIODISKA PRSKATSANA
91
12.4 RKRTAS APKOPE
91
12.5 KALPOSANAS LAIKS
91
13. BOJJUMU NOVRSANAS TABULA
92
14. PIEDERUMI
92
15. REZERVES DAAS
92
16. UTILIZCIJA
92
6
/
ZH 1. 2.
93 93
2.1
93
2.2
93
2.3
93
2.4
93
2.5
93
2.5.1
93
2.5.2
93
3.
93
4.
93
4.1
93
4.2
93
4.3
94
4.4
94
5. /
94
6.
94
7.
95
8.
95
9.
95
10.
95
11.
95
11.1
95
12.
96
12.1
96
12.2
96
12.3
96
12.4
96
12.5
96
13.
96
14.
96
15.
96
16.
96
JA 1. 2.
97 97
2.1
97
2.2
97
2.3
97
2.4
97
2.5
97
2.5.1
97
2.5.2
97
3.
97
4.
97
4.1
97
4.2
97
4.3
98
4.4
98
5. /
98
6.
99
7.
99
8.
99
9.
99
10.
100
11.
100
11.1
100
12.
100
12.1
100
12.2
100
12.3
100
12.4
100
12.5
101
13.
101
14.
101
15.
101
16.
101
7
IT EN DE FR ES PT EL RO CS BG
1. MODELLI I modelli base riportati di seguito possono essere soggetti a implementazioni o modifiche senza preavviso.
· T-Straps
· Pin Straps
· Reflex Straps
· ECS Straps
· Rock Straps
· RSP Straps
2. DESTINAZIONE D’USO
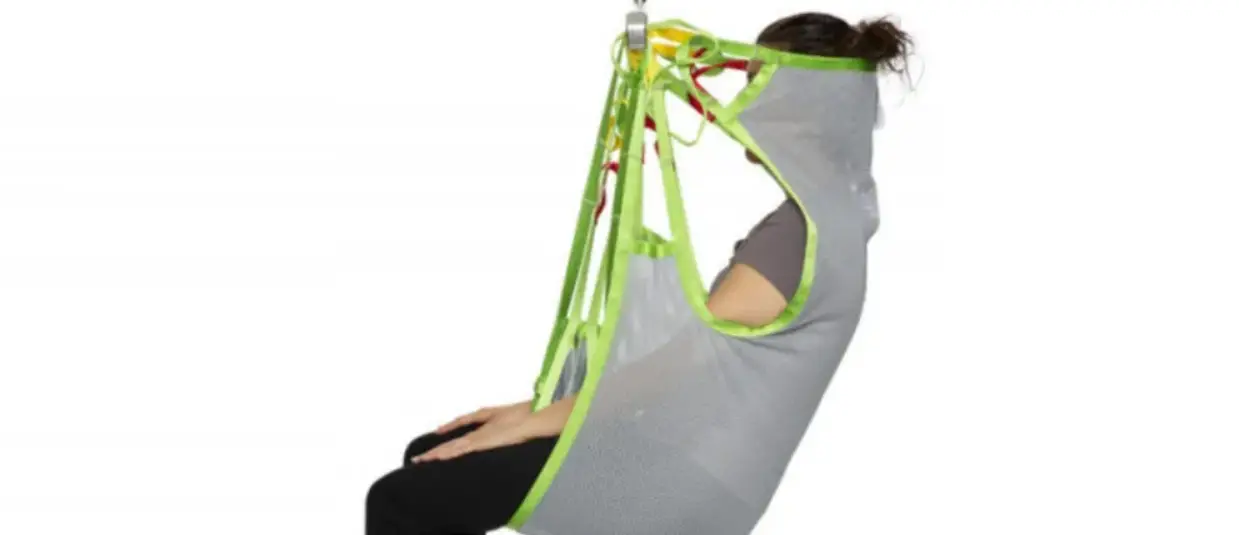
2.1 DESTINAZIONE D’USO E BENEFICI CLINICI Le cinture di trattenuta integrale sono ausili da utilizzarsi per immobilizzare il paziente su tavole spinali Spencer.
2.2 PAZIENTI DESTINATARI Non sono presenti particolari indicazioni legate al gruppo di pazienti. La conformazione del prodotto, consente l’utilizzo con qualunque soggetto purché nei limiti delle dimensioni del dispositivo. Qualora debbano essere trasportati soggetti pediatrici, sarà nel ruolo del soccorritore stabilire se i sistemi di cinture siano idonei alla sua immobilizzazione o se sarà invece necessario utilizzare un altro presidio.
2.3 CRITERI DI SELEZIONE PAZIENTI
I criteri di selezione dei pazienti attesi sono quelli applicabili al dispositivo con cui la cintura viene utilizzata.
2.4 CONTROINDICAZIONI ED EFFETTI COLLATERALI INDESIDERATI
Non sono note particolari controindicazioni o effetti collaterali derivanti dall’uso del dispositivo, purché utilizzato in accordo al manuale d’uso.
2.5 UTILIZZATORI E INSTALLATORI
Gli utilizzatori previsti, sono addetti al soccorso, esperti nella movimentazione, immobilizzazione e trasporto del paziente. I dispositivi non sono destinati ad utilizzatori profani.
Le cinture di trattenuta integrale sono un dispositivo destinato esclusivamente all’uso professionale. Non consentire a persone non addestrate di aiutare durante l’uso del prodotto, poiché potrebbero causare lesioni a se stessi o ad altre persone. Malgrado tutti gli sforzi, i test di laboratorio, i collaudi, le istruzioni d’uso, le norme non sempre riescono a riprodurre la pratica, per cui i risultati ottenuti nelle reali condizioni di utilizzo del prodotto nell’ambiente naturale possono differire in maniera talvolta anche rilevante Le migliori istruzioni sono la continua pratica d’uso sotto la supervisione di personale competente e preparato
Gli operatori che lo utilizzano devono possedere capacità fisica nell’utilizzare il dispositivo e buona coordinazione muscolare. Le capacità degli operatori devono essere valutate prima della definizione dei ruoli nell’impiego del dispositivo. Gli operatori devono essere in grado di fornire la necessaria assistenza al paziente.
2.5.1 FORMAZIONE UTILIZZATORI · Indipendentemente dal livello di esperienza acquisito in passato con dispositivi analoghi, è necessario leggere con attenzione e comprendere il contenuto del presente
manuale prima dell’installazione, della messa in uso del prodotto o di qualsiasi intervento di manutenzione. In caso di dubbi, interpellare Spencer Italia S.r.l. per ottenere i necessari chiarimenti. · Il prodotto deve essere utilizzato solamente da personale addestrato all’utilizzo di questo prodotto e non di altri analoghi. · L’idoneità degli utilizzatori all’uso del prodotto può essere attestata con la registrazione della formazione, nella quale sono specificate persone formate, formatori, data e luogo. Tale documentazione deve essere mantenuta almeno per 10 anni dal fine vita del prodotto e deve essere messa a disposizione delle Autorità competenti e/o del Fabbricante, quando richiesto. In mancanza, gli organi preposti applicheranno eventuali sanzioni previste. · Non consentire a persone non addestrate di aiutare durante l’uso del prodotto, poiché potrebbero causare lesioni a se stessi o ad altre persone. Nota: Spencer Italia S.r.l. si ritiene sempre a disposizione per lo svolgimento di corsi di formazione.
2.5.2 FORMAZIONE INSTALLATORE
Non è prevista installazione.
DA FI NL NO SV SR LV ZH
3. STANDARD DI RIFERIMENTO
In qualità di Distributore o Utilizzatore finale dei prodotti fabbricati e/o commercializzati da Spencer Italia S.r.l., è rigorosamente richiesto di conoscere le disposizioni di legge in vigore nel Paese di destinazione della merce, applicabili ai dispositivi oggetto della fornitura (ivi comprese le normative relative alle specifiche tecniche e/o ai requisiti di sicurezza) e, pertanto, di conoscere gli adempimenti necessari per assicurare la conformità dei medesimi prodotti a tutti i requisiti di legge del territorio.
RIFERIMENTO Regolamento UE 2017/745
TITOLO DEL DOCUMENTO Regolamento UE relativo ai Dispositivi Medici
4. INTRODUZIONE
4.1 UTILIZZO DEL MANUALE Il presente Manuale ha lo scopo di fornire all’operatore sanitario le informazioni necessarie per un utilizzo sicuro ed appropriato e per un’adeguata manutenzione del dispositivo.
Nota: il Manuale è parte integrante del dispositivo, pertanto deve essere conservato per tutta la durata del dispositivo e dovrà accompagnare lo stesso in eventuali cambi di destinazione o di proprietà. Nel caso in cui fossero presenti istruzioni d’uso relative ad altro prodotto, diverso da quello ricevuto, è necessario contattare immediatamente il Fabbricante prima dell’uso. I Manuali d’Uso dei prodotti Spencer, possono essere scaricati dal sito http://support.spencer.it oppure contattare il Fabbricante. Fanno eccezione gli articoli la cui essenzialità ed un uso ragionevole e prevedibile siano tali da non rendere necessaria la stesura di istruzioni, in aggiunta alle seguenti avvertenze ed alle indicazioni riportate sull’etichetta.
Indipendentemente dal livello di esperienza acquisito in passato con dispositivi analoghi, si raccomanda di leggere con attenzione il presente manuale prima dell’installazione, della messa in uso del prodotto o di qualsiasi intervento di manutenzione.
4.2 ETICHETTATURA E CONTROLLO TRACCIABILITÀ DEL DISPOSITIVO
Ogni dispositivo viene dotato di un’etichetta, posizionata sul dispositivo stesso e/o sulla confezione, nella quale sono presenti i dati identificativi del Fabbricante, del prodotto, marcatura CE, numero di matricola (SN) o lotto (LOT). Questa non deve essere mai rimossa o coperta. In caso di danneggiamento o rimozione richiedere il duplicato al Fabbricante, pena la validità della garanzia, poiché il dispositivo non potrà più essere rintracciato. Qualora non si riesca a risalire al lotto/SN assegnato è necessario effettuare il ricondizionamento del dispositivo, previsto solo sotto la responsabilità del fabbricante.
Il Regolamento UE 2017/754 richiede ai produttori e ai distributori di dispositivi medici di tenere traccia della loro ubicazione. Se il dispositivo si trova in una sede diversa dall’indirizzo a cui è stato spedito oppure è stato venduto, donato, perduto, rubato, esportato o distrutto, rimosso permanentemente dall’uso, oppure se il dispositivo non è stato consegnato direttamente da Spencer Italia S.r.l. registrare il dispositivo all’indirizzo http://service.spencer.it, oppure informare l’Assistenza Clienti (cfr. § 4.4).
JA
8
4.3 SIMBOLI Simbolo Significato Dispositivo conforme al Regolamento UE 2017/745 Dispositivo medico Fabbricante Data di fabbricazione Unique Device Identifier
(01)8057711230006 (11) 200626 (10) 1234567890
Simbolo
Significato
Pericolo Indica una situazione di pericolo che può comportare una situazione direttamente connessa a lesioni gravi o letali
Consultare il manuale d’uso
Numero di lotto
Codice del prodotto
Attenzione: La legge federale limita questo dispositivo alla vendita da o su ordine di un medico autorizzato (solo per il mercato USA)
Identificativo della produzione Codice alfanumerico che identifica le unità di produzione del dispositivo, composta da:
(01)805771123 000 6
(11)200626 (10)1234567890
prefisso aziendale progressivo GS1 numero di controllo
data di produzione (YYMMDD) numero di lotto
IT EN DE FR ES
4.4 GARANZIA E ASSISTENZA Spencer Italia S.r.l. garantisce che i prodotti sono senza difetti per un periodo di un anno a partire dalla data dell’acquisto.
Per informazioni relative alla corretta interpretazione delle istruzioni, all’uso, alla manutenzione, all’installazione o al reso, contattare l’ Assistenza Clienti Spencer tel. +39 0521 541154, fax +39 0521 541222, e-mail [email protected]. Per agevolare le operazioni di assistenza, indicare sempre il numero di lotto (LOT) o matricola (SN) riportato sull’etichetta applicata alla confezione o al dispositivo stesso. Condizioni di garanzia e assistenza sono disponibili al sito http://support.spencer.it.
Nota: Registrare e conservare con queste istruzioni: lotto (LOT) o matricola (SN) se presente, luogo e data di acquisto, data primo utilizzo, data controlli, nome degli utilizzatori e commenti.
5. AVVERTENZE/PERICOLI
Le avvertenze, i pericoli, le note ed altre importanti informazioni di sicurezza sono riportati in questa sezione e chiaramente visibili in tutto il manuale. Almeno ogni 6 mesi, è importante verificare la presenza di istruzioni aggiornate ed eventuali modifiche che coinvolgano il proprio prodotto. Queste informazioni, sono liberamente consultabili sul sito www.spencer.it nella pagina dedicata al prodotto.
Funzionalità prodotto
È vietato l’impiego del prodotto per qualsiasi altro utilizzo diverso da quello descritto nel Manuale d’Uso.
Prima di ogni utilizzo verificare sempre l’integrità del prodotto, come specificato nel Manuale d’Uso ed in caso di anomalie/danni che possano comprometterne la funzionalità/sicurezza, è necessario toglierlo immediatamente dal servizio e contattare il Fabbricante.
Il prodotto non deve subire alcuna manomissione e modifica senza l’autorizzazione del fabbricante (modifica, ritocco, aggiunta, riparazione), poiché possono costituire imminenti pericoli di lesione a persone nonché danni materiali. In caso contrario si declina ogni responsabilità sul funzionamento non corretto o su eventuali danni provocati dal prodotto stesso; inoltre si rendono nulle la marcatura CE e la garanzia del prodotto Assicurarsi di aver adottato ogni precauzione al fine di evitare pericoli derivanti dal contatto con sangue o secreti corporei, se applicabile. · Nel caso di ravvisato malfunzionamento del prodotto, utilizzare immediatamente un dispositivo analogo, per garantire la continuità delle operazioni in corso. Il dispositivo non conforme deve essere messo fuori uso. · Durante l’utilizzo dei dispositivi, posizionarli e regolarli in modo tale da non ostacolare le operazioni degli operatori e l’utilizzo di eventuali altre apparecchiature. · Evitare il contatto con oggetti taglienti o abrasivi. · Temperatura di utilizzo: da -5°C a + 50°C.
Stoccaggio · Il prodotto non deve essere esposto, né venire in contatto con fonti termiche di combustione ed agenti infiammabili, ma deve essere stoccato in luogo asciutto, fresco, al
riparo dalla luce e dal sole. · Non stoccare il prodotto sotto altri materiali più o meno pesanti, che possano danneggiare il dispositivo. · Stoccare e trasportare il prodotto con la sua confezione originale, in caso contrario la garanzia risulta invalidata. · Temperatura di stoccaggio: da -10°C a +60°C.
Requisiti regolatori
In qualità di Distributore o Utilizzatore finale dei prodotti fabbricati e/o commercializzati da Spencer Italia S.r.l., è rigorosamente richiesto di conoscere le disposizioni di legge in vigore nel Paese di destinazione della merce, applicabili ai dispositivi oggetto della fornitura (ivi comprese le normative relative alle specifiche tecniche e/o ai requisiti di sicurezza) e, pertanto, di conoscere gli adempimenti necessari per assicurare la conformità dei medesimi prodotti a tutti i requisiti di legge del territorio.
· Informare tempestivamente e dettagliatamente Spencer Italia S.r.l. (già in fase di richiesta preventivo) circa eventuali adempimenti a cura del Fabbricante necessari per la conformità dei prodotti agli specifici requisiti di legge del territorio (ivi inclusi quelli derivanti da regolamenti e/o disposizioni normative di altra natura).
· Agire, con la debita cura e diligenza, per contribuire a garantire la conformità ai requisiti generali di sicurezza dei dispositivi immessi sul mercato, fornendo agli utilizzatori finali tutte le informazioni necessarie per lo svolgimento delle attività di revisione periodica sui dispositivi in dotazione, esattamente come indicato nel Manuale d’Uso.
· Partecipare al controllo di sicurezza del prodotto immesso sul mercato, trasmettendo le informazioni concernenti i rischi del prodotto al Fabbricante nonché alle Autorità Competenti per le azioni di rispettiva competenza.
· Fermo quanto sopra, il Distributore o Utilizzatore finale, assume sin d’ora ogni più ampia responsabilità collegata al mancato adempimento dei sopra indicati incombenti con conseguente obbligo di tenere indenne e/o manlevare Spencer Italia S.r.l. da ogni, eventuale, relativo effetto pregiudizievole.
· In riferimento al Regolamento UE 2017/745, si ricorda che gli operatori pubblici o privati, che nell’esercizio della loro attività rilevano un incidente che coinvolga un prodotto medico sono tenuti a darne comunicazione al Ministero della salute, nei termini e con le modalità stabilite con uno o più decreti ministeriali, e al Fabbricante. Gli operatori sanitari pubblici o privati sono tenuti a comunicare al Fabbricante, ogni altro inconveniente che possa consentire l’adozione delle misure atte a garantire la protezione e la salute dei pazienti e degli utilizzatori.
Avvertenze generali per dispositivi medici
L’utilizzatore deve leggere attentamente, in aggiunta alle avvertenze generali, anche quelle di seguito elencate.
· Non è previsto che l’applicazione del dispositivo duri oltre il tempo necessario alle operazioni di primo intervento e le successive fasi di trasporto fino al punto di soccorso più vicino.
PT EL RO CS BG DA FI NL NO SV SR LV ZH JA
9
IT EN DE FR ES PT EL
Non utilizzare se il dispositivo o sue parti sono forate, strappate, sfilacciate o eccessivamente usurate. Non alterare o modificare arbitrariamente il dispositivo la modifica potrebbe provocarne il funzionamento imprevedibile e danni al paziente o ai soccorritori e comunque la perdita della garanzia e sollevando il Fabbricante da qualsiasi responsabilità · Durante l’utilizzo del dispositivo deve essere garantita l’assistenza di personale qualificato e devono essere presenti almeno due operatori. · Seguire le procedure ed i protocolli interni approvati dalla propria organizzazione. · Le attività di disinfezione devono essere eseguite in accordo ai parametri di ciclo validato, riportati nelle norme tecniche specifiche. · Non utilizzare macchine asciugatrici per asciugare il dispositivo. · Nel caso di cute esposta e/o lesa, coprire le superfici a contatto col paziente con un lenzuolo chirurgico che rispetti le normative di biocompatibilità per tutelare la salute del paziente.
6. AVVERTENZE SPECIFICHE
Per l’utilizzo delle cinture di trattenuta integrali, è necessario anche aver letto, compreso e seguire accuratamente tutte le indicazioni presenti nel manuale d’uso.
· Rispettare sempre le specifiche di posizionamento determinate dal dispositivo con cui sono utilizzate le cinture. Inoltre, l’operatore deve valutare che l’ingombro del paziente non riduca la funzionalità del prodotto.
· Applicare sempre il numero di cinture previsto dal presidio di trasporto in uso. · Stabilire un programma di manutenzione e controlli periodici, identificando un addetto di riferimento. Il soggetto a cui viene affidata la manutenzione ordinaria del disposi-
tivo deve garantire i requisiti di base previsti dal fabbricante, all’interno delle presenti istruzioni d’uso. · Tutte le attività di manutenzione devono essere registrate e documentate con i relativi report di intervento tecnico le documentazione dovrà essere mantenuta almeno per
10 anni dal fine vita del dispositivo e dovrà essere messa a disposizione delle Autorità competenti e/o del fabbricante, quando richiesto.
Effettuare delle simulazioni di soccorso con le cinture applicate al prodotto con cui ne è previsto l’impiego e un carico simulante paziente e accessori, prima della messa in servizio del dispositivo. Prima di ogni utilizzo verificare sempre l’integrità del dispositivo e delle sue componenti, come specificato nel manuale d’uso. In caso di anomalie o danni che possano compromettere la funzionalità e la sicurezza del dispositivo, quindi del paziente e dell’operatore, è necessario mettere fuori servizio il dispositivo. Seguire le procedure approvate dal Servizio Medico d’Emergenza per il posizionamento e il trasporto del paziente. · Evitare il contatto con oggetti taglienti. · Seguire le procedure approvate dal Servizio Medico d’Emergenza per l’immobilizzazione e il trasporto del paziente. · Per preservare la vita del dispositivo è necessario proteggerlo il più possibile dai raggi UV e dalle condizioni meteo avverse. · Accertarsi che le fibbie siano adeguatamente ancorate al nastro e che siano integre e funzionanti.
RO
7. RISCHIO RESIDUO Non sono identificati rischi residui, ovvero rischi che si potrebbero originare nonostante il rispetto di tutte le avvertenze del presente manuale d’uso.
CS BG DA
8. DATI TECNICI E COMPONENTI Nota: Spencer Italia S.r.l. si riserva il diritto di apportare modifiche alle specifiche senza darne preavviso.
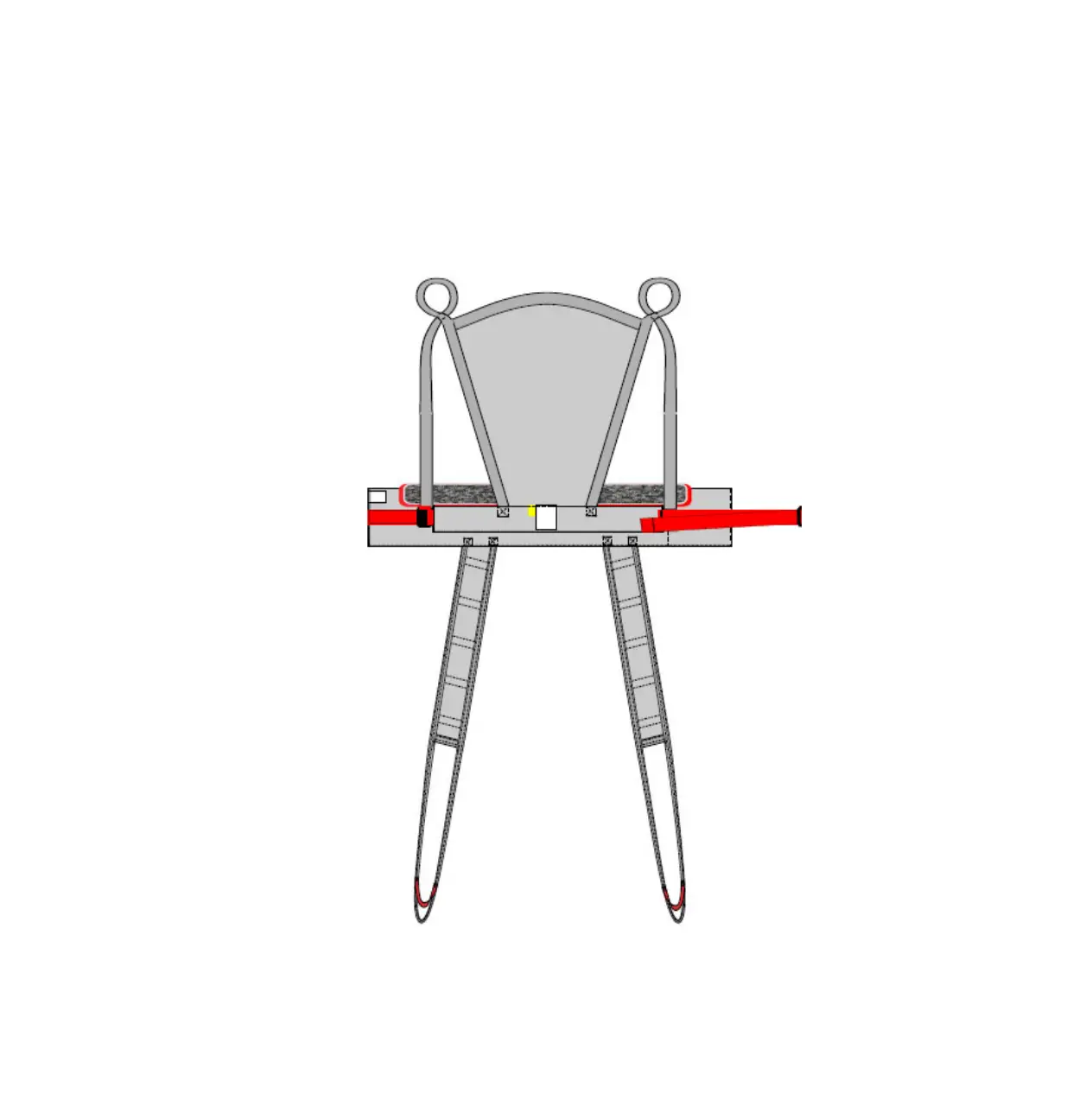
DESCRIZIONE
1 Moschettoni per Pin (se presenti)
2 Nastri trasversali con strap
3 Nastro longitudinale
FI NL NO
4 Nastri a “V”
N° Nastri Tipo fissaggio Materiale Peso
ROCK STRAPS 10
Strap
Polipropilene/Nylon 600g
T-STRAPS 10
Strap
Polipropilene/Nylon 800g
REFLEX STRAPS 10
Strap
Polipropilene/Nylon 600g
PIN STRAPS
10
Strap+moschettoni in metallo
Polipropilene/Nylon/Lega metallica
1500g
ECS STRAPS 12
Strap
Polipropilene/Nylon 800g
RSP STRAPS 10
Strap
Polipropilene/Nylon 350g
SV SR LV ZH JA
9. MESSA IN FUNZIONE
Per il primo utilizzo, verificare che:
· L’imballo sia integro e abbia protetto il dispositivo durante il trasporto · Controllare che siano presenti tutti i pezzi compresi nella lista di accompagnamento. · Funzionalità generale del dispositivo · Stato di pulizia del prodotto · Assenza di tagli, fori, lacerazioni o abrasioni sull’intera struttura · Stato di usura del dispositivo. · Verificare il corretto scorrimento dei nastri · Verificare il corretto funzionamento dei moschettoni se presenti nel modello · Verificare la corretta adesione degli inserti strap
Verificare al paragrafo 11 le modalità d’uso per lo svolgimento delle verifiche sopra indicate. Non modificare per nessun motivo il dispositivo nelle sue parti perché ciò potrebbe essere causa di danni al paziente e/o ai soccorritori.
La mancanza delle misure sopra indicate, preclude la sicurezza nell’uso del dispositivo, con il conseguente rischio di danni per il paziente, gli operatori e il dispositivo stesso. Per utilizzi successivi, effettuare le operazioni specificate al paragrafo 12.
Se le condizioni riportate sono rispettate, il dispositivo può essere considerato pronto all’uso; in caso contrario è necessario togliere immediatamente il dispositivo dal servizio e contattare il Fabbricante.
10
10. CARATTERISTICHE FUNZIONALI
Per le caratteristiche di funzionamento, consultare il paragrafo 11 Modalità d’uso.
11. MODALITA’ D’USO
Prima di intervenire sul paziente, devono essere effettuate delle valutazioni mediche primarie. Prima di utilizzare qualsiasi tipologia di cintura descritta nel presente manuale, leggere attentamente le istruzioni d’uso del dispositivo con cui è previsto il loro impiego.
11.1 APPLICAZIONE DELLE CINTURE
Seguire le procedure approvate dal Servizio Medico d’Emergenza di riferimento per l’immobilizzazione, il posizionamento ed il trasporto del paziente. Le procedure di seguito indicate sono redatte in base a informazioni generiche d’uso. 1. Il paziente si trova posizionato su tavola spinale con collare cervicale 2. Mantenendo sempre adeguata immobilizzazione, appoggiare la cintura sul paziente, disponendo i nastri a “V” circa 2/3 cm al di sotto del collare cervicale 3. Posizionare gli altri nastri trasversali in questo modo: · la cinghia toracica all’altezza del torace appena sotto le spalle · la cinghia pelvica all’altezza delle creste iliache · la prima cinghia degli arti inferiori sul femore, in prossimità del ginocchio · la seconda cinghia degli arti inferiori sulle tibie, in prossimità delle caviglie (se il paziente è basso arrotolare le cinghie) Prestare sempre la massima attenzione ad eventuali zone che possano aver subito traumi e/o fratture.
4. Applicare eventuali fermacapo e/o fermacaviglie se necessario. 5. Partendo dalle spalle verso i piedi, inserire le cinghie nei fori corrispondenti contemporaneamente sui due lati della spinale, utilizzando gli eventuali moschettoni che, se presenti, devono essere agganciati ai pin della tavola spinale. 6. Fissare le cinghie applicando una trazione uguale da entrambi i lati, dalle spalle verso i piedi e ponendo attenzione ad eventuali problemi respiratori ed addominali; 7. Assicurarsi che il paziente sia adeguatamente immobilizzato, quindi proseguire le manovre in accordo alle linee guida del Servizio medico d’emergenza di riferimento.
La cintura pediatrica RSP, destinata all’utilizzo con la tavola spinale Baby Go, è dotata di un metro con aree colorate, le quali consentono di identificare più rapidamente il lato che con buona probabilità risulterà più adeguato al paziente in relazione alla sua altezza. Il soccorritore è tuttavia l’unico responsabile della scelta del dispositivo e della sua corretta applicazione.
IT EN DE FR ES PT EL
12. PULIZIA E MANUTENZIONE
Spencer Italia S.r.l. declina ogni responsabilità per qualsiasi danno, diretto o indiretto, che sia conseguenza di un utilizzo improprio del prodotto e dei pezzi di ricambio e/o comunque diqualsiasi intervento di riparazione effettuato da soggetto diverso dal Fabbricante, che si avvale di tecnici interni ed esterni specializzati a ciòautorizzati; inoltre la garanzia risulta invalidata.
· Durante tutte le operazioni di controllo, manutenzione ed igienizzazione l’operatore deve indossare adeguati dispositivi di protezione individuali, quali guanti, occhiali, etc. · Stabilire un programma di manutenzione, controlli periodici e proroga del tempo di vita medio, se previsto dal Fabbricante nel Manuale d’Uso, identificando un addetto di
riferimento, che sia in possesso dei requisiti di base definiti nel Manuale d’Uso. · La frequenza dei controlli è determinata da fattori quali le prescrizioni di legge, il tipo di utilizzo, la frequenza di utilizzo, le condizioni ambientali durante l’uso e lo
stoccaggio. · La riparazione dei prodotti realizzati da Spencer Italia S.r.l. deve essere necessariamente effettuata dal Fabbricante, che si avvale di tecnici interni o esterni specializzati i
quali,utilizzando ricambi originali, forniscono un servizio di riparazione di qualitàin stretta conformità alle specifiche tecniche indicatedal Produttore. Spencer Italia S.r.l. declina ogni responsabilità per qualsiasi danno, diretto o indiretto, che sia conseguenza di un utilizzo improprio dei pezzi di ricambio e/o comunque diqualsiasi intervento di riparazione effettuato da soggetti non autorizzati. · Il ricondizionamento, processo eseguito sul dispositivo per consentirne il ripristino della sicurezza tecnica e funzionale del dispositivo usato, esempio reimmatricolazione, deve essere eseguito dal Fabbricante. · Tutte le attività di manutenzione e revisione devono essere registrate e documentate con i relativi report di intervento tecnico; la documentazione dovrà essere mantenuta almeno per 10 anni dal fine vita del prodotto e dovrà essere messa a disposizione delle Autorità competenti e/o del Fabbricante, quando richiesto. · La pulizia, prevista per i prodotti riutilizzabili, deve essere eseguita nel rispetto delle indicazioni fornite dal Fabbricante nel Manuale d’Uso, al fine di evitare il rischio di infezioni crociate dovute alla presenza di secreti e/o residui.
12.1 PULIZIA
La mancata esecuzione delle operazioni di pulizia può comportare il rischio di infezioni crociate dovute alla presenza di secreti e/o residui. Durante tutte le operazioni di controllo e igienizzazione l’operatore deve indossare adeguati dispositivi di protezione individuali, quali guanti, occhiali etc.
Lavare le parti esposte con acqua tiepida e sapone neutro; non usare mai solventi o smacchianti. Risciacquare accuratamente con acqua tiepida verificando di avere eliminato ogni traccia di detergente, che potrebbe deteriorarla o comprometterne l’integrità e la durata. L’uso di acqua ad alta pressione deve essere evitato. Lasciare asciugare perfettamente prima di riporla. L’asciugatura dopo il lavaggio oppure dopo l’utilizzo in ambiente umido deve essere naturale e non forzata; non utilizzare fiamme o altre fonti di calore diretto. In presenza di sangue, ossidarlo prima di procedere al lavaggio con acqua. Blue splint, può essere lavata in lavatrice a 40°C, previa rimozione dell’anima metallica. Nel caso di eventuale disinfezione utilizzare prodotti che, oltre ad essere classificati come presidi medico-chirurgici, non abbiano azione solvente o corrosiva su materiali costituenti il dispositivo. Assicurarsi di aver preso tutte le precauzioni idonee a garantire che non sussistano rischi di infezioni crociate o contaminazioni di pazienti e operatori.
12.2 MANUTENZIONE ORDINARIA
E’ necessario stabilire un programma di controlli periodici, identificando un addetto di riferimento. Il soggetto a cui viene affidata la manutenzione del dispositivo deve garantire i requisiti di base previsti nel presente manuale d’uso. Tutte le attività di manutenzione, devono essere registrate e documentate con i relativi report di intervento tecnico. Tale documentazione dovrà essere mantenuta almeno per 10 anni dal fine vita del dispositivo e dovrà essere messa a disposizione delle Autorità competenti e/o del Fabbricante, quando richiesto.
Durante tutte le operazioni di controllo, manutenzione ed igienizzazione l’operatore deve indossare adeguati dispositivi di protezione individuali, quali guanti, occhiali, etc.
Il dispositivo non richiede un programma di manutenzione ordinaria, ma è necessario effettuare controlli intesi a verificare: · Funzionalità generale del dispositivo · Stato di pulizia del dispositivo (si ricorda che la mancata esecuzione delle operazioni di pulizia può comportare il rischio di infezioni crociate) · Soddisfacimento dei requisiti previsti dal manuale d’uso nella sezione 5 Avvertenze e 6 Avvertenze specifiche · Soddisfacimento dei requisiti previsti dal manuale nella sezione 11 Modalità d’uso
Utilizzare solo componenti/ parti di ricambio e/o accessori originali o approvati da Spencer Italia S.r.l., in modo da effettuare ogni operazione senza causare alterazioni, modifiche al dispositivo; in caso contrario si declina ogni responsabilità sul funzionamento non corretto o su eventuali danni provocati dal dispositivo stesso al paziente o all’operatore, invalidandone la garanzia e facendo decadere la conformità al Regolamento UE 2017/745.
12.3 REVISIONE PERIODICA
Non è prevista una revisione periodica per il dispositivo.
RO CS BG DA FI NL NO SV SR LV ZH JA
11
IT EN
12.4 MANUTENZIONE STRAORDINARIA La manutenzione straordinaria può essere eseguita solo dal Fabbricante, che si avvale di tecnici interni ed esterni specializzati ed autorizzati dal Fabbricante stesso.
Si intendono validate da Spencer Italia S.r.l. solo le attività di manutenzione svolte da tecnici specializzati ed autorizzati dal Fabbricante. 12.5 TEMPO DI VITA
Il dispositivo, se utilizzato come riportato nelle seguenti istruzioni, ha un tempo di vita di 5 anni dalla data di acquisto.
Spencer Italia S.r.l. declina ogni responsabilità sul funzionamento non corretto o su eventuali danni provocati dall’utilizzo di dispositivi che abbiano superato il tempo di vita massimo ammesso.
DE FR ES PT EL RO CS
13. TABELLA GESTIONE GUASTI
PROBLEMA
CAUSA
RIMEDIO
Non è possibile agganciare il moschettone al pin presente sulla tavola spinale
Il moschettone è danneggiato oppure dei detriti ne ostacolano l’apertura
Verificare che nulla interferisca con l’apertura. Se tutto risulta pulito ed il problema non è stato risolto, mettere immediatamente il dispositivo fuori servizio e contattare il fabbricante
La cintura non si chiude
Aree strap sporche o distaccate
Pulire le aree strap e verificarne la corretta adesione.
Se il problema persiste, mettere il dispositivo fuori servizio e contattare il fabbricante
Nel caso il problema o guasto rilevato non corrisponda a quanto sopra indicato contattare il servizio assistenza Spencer Italia srl.
14. ACCESSORI Non sono presenti accessori per questi dispositivi.
15. RICAMBI Non sono presenti ricambi per questi dispositivi.
16. SMALTIMENTO Una volta inutilizzabili i dispositivi, ed i loro accessori, qualora non siano stati contaminati da agenti particolari, possono essere smaltiti come normali rifiuti solidi urbani, altrimenti attenersi alle norme vigenti in materia di smaltimento.
BG
DA
FI
NL
NO
SV
SR
LV
ZH JA
Avvertenza
Le informazioni contenute in questo documento sono soggette a modifica senza preavviso e sono da intendersi come impegno da parte della Spencer Italia S.r.l. con riserva di modifiche. Le immagini sono inserite a titolo di esempio e possono variare da quelle vere e proprie del dispositivo.
© Copyright Spencer Italia S.r.l. Tutti i diritti sono riservati. Nessuna parte del documento può essere fotocopiata, riprodotta o tradotta in un’altra lingua senza previo consenso scritto della Spencer Italia S.r.l.
12
1. MODELS The following basic models may be subject to implementation or change without notice.
· T-Straps
· Pin Straps
· Reflex Straps
· ECS Straps
· Rock Straps
· RSP Straps
2. INTENDED USE
2.1 INTENDED USE AND CLINICAL BENEFITS
Full body restraint belts are aids used to immobilise patients on Spencer spine boards.
2.2 TARGET PATIENTS There are no particular indications related to the patient group. The design of the product allows it to be used with any person within the dimensions of the device. If paediatric subjects must be transported, it will be in the role of the rescuer to determine whether the belt systems are suitable for immobilization or if it will be necessary to use another device.
2.3 PATIENT SELECTION CRITERIA
The expected patient selection criteria are those applicable to the device with which the belt is used.
2.4 CONTRAINDICATIONS AND UNWANTED SIDE EFFECTS
No particular contraindications or side effects are known with relation to use of the device, as long as it is used in accordance with the user manual.
2.5 USERS AND INSTALLERS
The intended users are rescue workers and experts in patient handling, immobilisation and transport. These devices are not intended for lay people.
Full body restraint belts are devices intended for professional use only. Do not allow untrained persons to help while using the product, as they may cause injury to themselves or others. Despite all efforts, laboratory tests, trials, and instructions for use, standards do not always reproduce practice, so the results obtained under actual conditions of product use in the natural environment may sometimes differ significantly. The best instructions are the continuous practice of use under the supervision of competent and trained personnel.
Operators using the device should be physically able to use the device and have good muscle coordination. Operators’ ability must be assessed before the definition of roles in use of the stretcher. Operators must be able to provide the necessary patient care.
2.5.1 USER TRAINING · Regardless of your level of experience with similar devices in the past, you should carefully read and understand the contents of this manual before installing, operating, or
servicing this product. In case of any questions, please contact Spencer Italia S.r.l. for the necessary clarifications. · The product must be used only by personnel trained in the use of this product and not on other similar products. · The suitability of the users for use of this product can be attested by the training registration, in which trained persons, trainers, date and place are specified. This docu-
mentation must be kept for at least 10 years after the end of the product’s life and must be made available to the competent authorities and/or the Manufacturer when requested. In the absence of such documentation, the relevant bodies will apply any foreseen sanctions. · Do not allow untrained persons to help while using the product, as they may cause injury to themselves or others. Note: Spencer Italia S.r.l. is always available for training courses.
2.5.2 INSTALLER TRAINING
Installation is not required.
IT EN DE FR ES PT EL RO CS BG
3. REFERENCE STANDARDS
As Distributor or End-User of the products manufactured and/or marketed by Spencer Italia S.r.l., users are strictly required to be familiar with the legal provisions in force in the country of destination of the goods, applicable to the devices to be supplied (including regulations relating to technical specifications and/or safety requirements) and, therefore, to understand the requirements necessary to ensure compliance of the products themselves with all legal requirements of the territory.
REFERENCE EU Regulation 2017/745
DOCUMENT TITLE EU Regulation on Medical Devices
DA FI
4. INTRODUCTION
4.1 USING THE MANUAL
The purpose of this manual is to provide healthcare professionals with the information necessary for safe and appropriate use and maintenance of the device. Note: The Manual is an integral part of the device and therefore it must be kept for the entire life of the device and must accompany it in any changes of use or ownership. If any instructions for use for products other than the one received are present, please contact the Manufacturer immediately before use. Spencer products User Manuals can be downloaded from the site http://support.spencer.it or by contacting the Manufacturer. Exceptions are those items whose essentiality and reasonable and predictable use are such that it is not necessary to draw up instructions, in addition to the following warnings and indications on the label.
Regardless of your level of experience with similar devices in the past, it is advisable to carefully read and understand the contents of this manual before installing, operating, or servicing this product.
4.2 DEVICE LABELLING AND TRACEABILITY
Each device is provided with a label, placed on the device itself and/or on the packaging, which contains the Manufacturer’s identification data, product, CE marking, serial number (SN) or lot number (LOT). This must never be removed or covered. In the event of damage or removal, request a duplicate from the Manufacturer, or else the warranty will be void as the device can no longer be traced. If the assigned Lot/SN cannot be traced, the device must be reconditioned, provided only under the responsibility of the manufacturer.
EU Regulation 2017/754 requires manufacturers and distributors of medical devices to keep track of their location. If the device is in a location other than the address to which it was shipped or sold, or if it was donated, lost, stolen, exported or destroyed, permanently removed from use, or if the device was not delivered directly from Spencer Italia S.r.l., please register the device at http://service.spencer.it, or inform Customer Service (see § 4.4).
NL NO SV SR LV ZH
JA
13
IT EN DE
4.3 SYMBOLS Symbol Meaning Device in compliance with EU Regulation 2017/745 Medical device Manufacturer Date of manufacture Unique Device Identifier
FR
ES
(01)8057711230006 (11) 200626 (10) 1234567890
Symbol
Meaning Danger Indicates a hazardous situation that may result in a situation directly related to serious injury or death.
See the instructions for use
Lot number
Product code
Caution: Federal law restricts the sale of this device by or on the order of a licensed professional (US market only)
Production identification Alphanumeric code that identifies the production units of the device, composed of:
(01)805771123 000 6
(11)200626 (10)1234567890
company prefix progressive GS1 control number
date of production (YYMMDD) lot number
PT EL
4.4 WARRANTY AND SERVICE Spencer Italia S.r.l. guarantees that products are free from defects for a period of one year from the date of purchase.
For information regarding correct interpretation of the instructions for use, maintenance, installation or return, please contact Spencer Customer Service tel. +39 0521 541154, fax +39 0521 541222, e-mail [email protected]. To facilitate service, always indicate the lot number (LOT) or serial number (SN) on the label attached to the package or device itself. Warranty and service conditions are available at http://support.spencer.it. Note: Record and keep with these instructions: lot (LOT) or serial number (SN), if present, place and date of purchase, date of first use, date of checks, user name and comments.
RO CS BG DA FI NL NO SV SR LV ZH JA
5. WARNINGS/DANGERS
Warnings, dangers, notes, and other important safety information are provided in this section and are clearly visible throughout the manual. At least every 6 months, it is important to check for updated instructions and any changes involving your product. This information is freely available on the website www. spencer.it on the specific product page.
Product features
Use of the product for any purpose other than that described in the User Manual is prohibited.
Before each use, always check the conditions of the product, as specified in the User Manual. In the event of faults/damage that could compromise its functionality/safety, immediately remove it from service and contact the Manufacturer.
The product must not be tampered with or modified without the manufacturer’s authorisation (modification, tweaking, additions, repair), as they may constitute imminent danger of injury to persons and material damage. Should these operations be performed, we decline any responsibility for incorrect operation or any damage caused by the product itself; moreover, the CE marking and the product warranty shall be null and void Be sure to take every precaution to avoid hazards from contact with blood or body secretions, if applicable. · If the product is found to be malfunctioning, immediately use a similar device to ensure continuity of ongoing operations. Non-compliant devices must be taken out of service. · When using the devices, position and adjust them in such a way that they do not hinder operator works or the use of any other equipment. · Avoid contact with sharp or abrasive objects. · Operating temperature: from -5°C to + 50°C.
Storage · The product must not be exposed or come into contact with thermal sources of combustion or flammable agents, but must instead be stored in a dry, cool place, away
from light and sun. · Do not store the product under other more or less heavy materials that may damage the device. · Store and transport the product with its original packaging, otherwise the warranty shall be invalidated. · Storage temperature: -10°C to +60°C.
Regulatory requirements
As Distributor or End-User of the products manufactured and/or marketed by Spencer Italia S.r.l., users are strictly required to be familiar with the legal provisions in force in the country of destination of the goods, applicable to the devices to be supplied (including regulations relating to technical specifications and/or safety requirements) and, therefore, to understand the requirements necessary to ensure compliance of the products themselves with all legal requirements of the territory.
· Promptly and in detail notify Spencer Italia S.r.l. (already in the quotation request phase) about possible fulfilments by the Manufacturer necessary for the compliance of products with specific legal requirements of the territory (including those deriving from regulations and/or regulatory provisions of another nature).
· Act with due care and diligence to help ensure compliance with the general safety requirements of the devices placed on the market, providing end-users with all the information necessary to carry out periodic revisions on the supplied devices, exactly as indicated in the User Manual.
· Participate in safety checks on products placed on the market, transmitting information regarding product risks to the Manufacturer as well as to the Competent Authorities for their respective actions.
· Without prejudice to the above, the Distributor or End-User shall assume wider liability related to non-compliance with non-fulfilment of the above-mentioned obligations, with consequent obligation to indemnify and/or hold Spencer Italia S.r.l. harmless from any possible injurious effect.
· With reference to EU Regulation 2017/745, please note that public or private operators who, when exercising their activity, detect an incident involving a medical product are required to notify the Ministry of Health, within the terms and in the manner established by one or more ministerial decrees, and notify the Manufacturer. Public or private health care professionals are required to notify the Manufacturer of any other incident that may allow the adoption of measures to ensure the protection and health of patients and users.
General warnings for medical devices
The user must carefully read the following in addition to the general warnings.
· It is not foreseen that application of the device lasts longer than the time required for first aid operations and subsequent transport to the nearest rescue point.
14
Do not use if the device or parts of it are punctured, torn, frayed, or excessively worn. Do not alter or modify the device arbitrarily, as doing so could result in unpredictable operation and damage to the patient or rescuers and shall void the manufacturer’s warranty and release the manufacturer from all liability · Qualified personnel and at least two operators must be present during use of the device. · Follow the internal procedures and protocols approved by your organisation. · Disinfection operations must be carried out in accordance with the validated cycle parameters, as stated in the specific technical standards. · Do not use drying machines to dry the device. · In case of exposed and/or injured skin, cover the surfaces in contact with the patient with a surgical sheet that respects bio-compatibility regulations to protect the patient’s health.
IT EN
6. SPECIFIC WARNINGS
To use the full body restraint belts, you must also have read, understood and carefully follow all the instructions in the user manual.
· Always comply with the positioning specifications defined by the device with which the belts are used. In addition, the operator should assess whether the overall size of the patient reduces the functionality of the product.
· Always apply the number of belts provided by the transport equipment in use. · Establish a maintenance program and periodic checks, identifying a designated reference person. The person entrusted with routine maintenance of the device must ensure
the basic requirements envisaged by the manufacturer within these operating instructions. · All maintenance activities must be recorded and documented with the relevant technical operation reports. This documentation must be kept for at least 10 years after the
end of the device’s life and must be made available to the competent authorities and/or the manufacturer when requested.
Perform rescue simulations with the belts applied to the product with which it is intended to be used and a patient simulating load and accessories before putting the device into service. Before each use, always check the conditions of the device and its components, as specified in the user manual. In case of faults or damage that may compromise the functionality and safety of the device, and therefore the patient and the operator, remove the device from service. Follow approved Emergency Medical Service procedures for patient positioning and transportation. · Avoid contact with sharp objects. · Follow approved Emergency Medical Service procedures for patient immobilization and transportation. · To preserve the life of the device, protect it as much as possible from UV rays and adverse weather conditions. · Make sure that the buckles are properly anchored to the strap and that they are intact and functional.
DE FR ES PT EL
7. RESIDUAL RISK No residual risks, or rather risks that could arise despite compliance with all warnings in this user manual, have been identified.
8. TECHNICAL DATA AND COMPONENTS Note: Spencer Italia S.r.l. reserves the right to make changes to specifications without notice.
DESCRIPTION
1 Spring catches for Pins (if present)
2 Transversal belts with strap
3 Longitudinal belt
4 V-belts
RO CS BG DA FI
No. Belts Fastening type Material Weight
ROCK STRAPS 10
Strap
Polypropylene/Nylon 600g
T-STRAPS 10
Strap
Polypropylene/Nylon 800g
REFLEX STRAPS 10
Strap
Polypropylene/Nylon 600g
PIN STRAPS
10
Strap+metal spring catches
Polypropylene/Nylon/ Metal alloy 1500g
ECS STRAPS 12
Strap
Polypropylene/Nylon 800g
RSP STRAPS 10
Strap
Polypropylene/Nylon 350g
9. COMMISSIONING
For first use, check that:
· Packaging is intact and has protected the device during transportation · Check that all parts included in the packing list are present · General functionality of the device · Product cleanliness · Absence of cuts, holes, tears or abrasions on the entire structure · Conditions of wear of the device. · Check that the belts slide correctly, · Check that the spring catches are working correctly, if present on the model. · Check the correct adhesion of the strap inserts.
See paragraph 11 for how to carry out the above-mentioned checks. Do not modify the device or its parts for any reason as this could cause damage to the patient and/or rescuers.
Failure to take the above measures will preclude safe use of the device, resulting in risk of damage to the patient, operators and the device itself. For subsequent use, perform the operations specified in paragraph 12.
If the above conditions are met, the device may be considered ready for use; otherwise, you must immediately remove the device from service and contact the Manufacturer.
NL NO SV SR LV ZH JA
10. OPERATING CHARACTERISTICS See paragraph 11 – Proper use for operating characteristics.
15
IT EN DE FR ES PT
11. PROPER USE
Primary medical evaluations must be carried out before intervening on the patient. Before using any type of belt described in this manual, carefully read the operating instructions of the device with which it is intended to be used.
11.1 APPLYING THE BELTS
Follow approved Emergency Medical Service reference procedures for patient immobilization, positioning and transport. The following procedures are based on general usage information. 1. The patient is placed on a spine board with a cervical collar. 2. While maintaining adequate immobilization, place the belt on the patient, arranging the V-belts about 2/3 cm below the cervical collar. 3. Position the other transversal belts as follows: · The thorax strap at chest height just below the shoulders · The pelvic strap at the height of the iliac crests · The first leg strap on the femur, close to the knee · The second leg strap on the tibiae, close to the ankles (if the patient is short, roll up the straps) Always be extremely careful with any areas that may have suffered trauma and/or fractures.
4. Apply head restraints and/or ankle restraints if necessary. 5. Starting from the shoulders towards the feet, insert the straps into the corresponding holes on both sides of the spine at the same time, if necessary using the spring catches, which must be hooked onto the pins of the spine board. 6. Fasten the straps by applying equal traction on both sides, from the shoulders towards the feet, paying attention to any respiratory and abdominal problems; 7. Make sure that the patient is adequately immobilized, then continue the manoeuvres according to the guidelines of the relevant Emergency medical service.
The RSP paediatric belt, intended for use with the Baby Go spine board, is equipped with a tape measure with coloured areas which allow quicker identification of which side is most likely to be appropriate for the patient in relation to their height. The rescuer is however solely responsible for the choice of device and its correct application.
EL RO CS BG DA FI NL NO SV SR LV ZH JA
12. CLEANING AND MAINTENANCE
Spencer Italia S.r.l. declines all responsibility for any direct or indirect damage which is the consequence of improper use of the product and spare parts and/or in any case of any repair carried out by a person other than the Manufacturer, who uses internal and external technicians authorised to do so; moreover, doing so will invalidate the warranty.
· The operator must wear suitable personal protective equipment, such as gloves, goggles, etc. during all checking, maintenance and cleaning operations. · Establish a maintenance schedule, periodic inspections and extend the average life span, if foreseen by the Manufacturer in the User Manual, identifying a reference person
who meets the basic requirements set forth in the User Manual. · The frequency of inspections is determined by factors such as legal requirements, type of use, frequency of use, and environmental conditions during use and storage. · Repairs of products manufactured by Spencer Italia S.r.l. must be carried out by the Manufacturer, who shall make use of specialised internal or external technicians
who,using original spare parts, shall provide quality repair service in strict compliance with the technical specifications indicated by the Manufacturer. Spencer Italia S.r.l. declines any responsibility for any direct or indirect damage which is a consequence of improper use of spare parts and/or any repair work carried out by unauthorised parties. · Reconditioning, a process performed on the device to restore the technical and functional safety of the device used, for example re-registration, must be performed by the Manufacturer. · All maintenance and overhaul activities must be recorded and documented with the relevant technical operation reports. This documentation must be kept for at least 10 years after the end of the product’s life and must be made available to the competent authorities and/or the Manufacturer when requested. · Cleaning, provided for reusable products, must be carried out in accordance with the Manufacturer’s instructions in the User Manual in order to avoid the risk of cross-infection due to the presence of body fluids and/or residues.
12.1 CLEANING
Failure to carry out the correct cleaning operations could increase the risk of cross-infection due to presence of body fluids and/or residues. The operator must wear suitable personal protective equipment, such as gloves, goggles, etc. during all checking and cleaning operations.
Any metal parts exposed to external agents undergo surface treatments and/or coating in order to obtain better resistance. Clean the exposed parts with water and delicate soap. Never use solvents or stain removers. Rinse thoroughly with lukewarm water, making sure you have removed all traces of soap, which may deteriorate or compromise conditions and durability. Avoid using high pressure water. Let dry completely before storing. Drying after washing or after use in a wet environment must be natural and not forced. Do not use flames or other direct heat sources. If disinfecting, use products that do not have a solvent or corrosive action on materials constituting the device, in addition to being classified as medical-surgical devices. Be sure to take all precautions to ensure that there is no risk of cross-infection or contamination of patients and operators. In the case of disposable products, no cleaning is required except that the product be properly stored and packaged according to the manufacturer’s specifications.
12.2 ROUTINE MAINTENANCE
You must establish a program for periodic checks, identifying a designated reference person. The person entrusted with device maintenance must ensure the basic requirements envisaged within this user manual. All maintenance activities must be recorded and documented with the relevant technical intervention reports. This documentation must be kept for at least 10 years after the end of the device’s life and must be made available to the competent authorities and/or the Manufacturer when requested.
The operator must wear suitable personal protective equipment, such as gloves, goggles, etc. during all checking, maintenance and cleaning operations.
The device does not require a routine maintenance program, but checks must be made to verify: · General functionality of the device · Cleanliness of the device (remember that the failure of cleaning may cause the risk of cross infections) · Fulfilment of the requirements of the user manual in section 5 Warnings and 6 Specific Warnings. · Fulfilment of the requirements of the manual in section 11 Proper use
Use only original or Spencer Italia S.r.l. approved components/replacement parts and/or accessories to carry out any operation without causing alterations or modifications to the device. Otherwise, we decline all responsibility regarding incorrect operation or any damage caused by the device to the patient or the operator, invalidating the warranty and invalidating compliance with EU Regulation 2017/745.
12.3 PERIODIC OVERHAUL
No periodic overhaul is foreseen for the device.
12.4 SPECIAL MAINTENANCE
Special maintenance can only be carried out by the Manufacturer, who uses internal and external technicians specialised and authorised by the Manufacturer itself.
Only maintenance activities carried out by specialised technicians authorised by the Manufacturer are considered valid by Spencer Italia S.r.l.
16
12.5 LIFE SPAN The device, if used as described in the following instructions, has a life span of 5 years from the date of purchase.
Spencer Italia S.r.l. will accept no responsibility for incorrect operation or damage caused by the use of devices that have exceeded the maximum allowable life span.
13. TROUBLESHOOTING TABLE
PROBLEM
CAUSE
REMEDY
It is not possible to attach the spring catch The spring catch is damaged or dirt is
to the pin on the spine board.
obstructing the opening.
Check that nothing is interfering with the opening. If everything is clean and the problem has not been solved, immediately remove the device from service and contact the manufacturer.
The belt does not close.
Strap areas dirty or detached.
Clean the strap areas and check for proper adhesion. If the problem persists, remove the device from service and contact the manufacturer.
If a problem or fault is detected that does not correspond to the above, please contact Spencer Italia srl customer care service.
IT EN DE FR
14. ACCESSORIES There are no accessories for these devices.
ES
15. SPARE PARTS There are no spare parts available for these devices.
PT
16. DISPOSAL
When devices and their accessories are no longer suitable for use, they can be disposed of as normal municipal solid waste if they have not been contaminated by special agents. Otherwise, follow the regulations in force regarding disposal.
EL RO
CS
BG
DA
FI
NL
NO
SV
SR
LV
Warning
The information contained in this document is subject to change without notice and is to be intended as a commitment by Spencer Italia S.r.l. subject to change. The images are included as examples and may vary slightly from the actual device.
© Copyright Spencer Italia S.r.l. All rights reserved. No part of the document may be photocopied, reproduced or translated into another language without prior written consent from Spencer Italia S.r.l.
ZH JA
17
IT EN DE FR ES PT EL RO CS BG DA FI NL
1. MODELLE Die nachfolgenden Basismodelle können ohne Vorankündigung ergänzt oder geändert werden.
· T-Straps
· Pin Straps
· Reflex Straps
· ECS Straps
· Rock Straps
· RSP Straps
2. VERWENDUNGSZWECK
2.1 VERWENDUNGSZWECK UND KLINISCHER NUTZEN
Die Integral-Haltegurte sind Hilfsmittel, um den Patienten auf Spencer-Wirbelsäulenbrettern zu immobilisieren.
2.2 ZIELPATIENTEN
Es bestehen keine besonderen Indikationen für bestimmte Patientengruppen. Die Formgebung des Produkts erlaubt den Einsatz bei jedem, solange die Abmessungen des Geräts nicht überschritten werden. Falls Kinder transportiert werden müssen, ist es Aufgabe des Notfallsanitäters festzulegen, ob die Gurtsysteme für die Immobilisation geeignet sind, oder ob eine andere Schutzvorrichtung verwendet werden muss.
2.3 AUSWAHLKRITERIEN FÜR PATIENTEN
Die Auswahlkriterien für erwartete Patienten sind diejenigen, die für das Gerät gelten, mit dem der Gurt verwendet wird.
2.4 GEGENANZEIGEN UND UNERWÜNSCHTE NEBENWIRKUNGEN
Es bestehen keine Gegenanzeigen oder Nebenwirkungen durch den Gebrauch des Geräts, sofern es gemäß Handbuch angewendet wird:
2.5 ANWENDER UND TECHNIKER
Das vorgesehene Anwendungspersonal sind Rettungskräfte mit Erfahrung für die Bewegung, die Immobilisierung und den Transport des Patienten. Die Geräte sind nicht für unfachmännische Anwender bestimmt.
Die Integral-Haltegurte sind ausschließlich für den professionellen Gebrauch bestimmt. Nicht geschulte Personen dürfen während des Gebrauchs des Produkts keine Hilfe leisten, da dies zu Verletzungen an ihnen selbst oder an anderen führen könnte. Trotz aller Anstrengungen, Labortests, Abnahmeprüfungen und Gebrauchsanweisungen entsprechen die Bestimmungen nicht immer den praktischen Anwendungen, daher können Ergebnisse unter realen Gebrauchsbedingungen des Produkts im Einsatzfeld mitunter deutlich von ihnen abweichen. Die besten Anleitung ist der stete Gebrauch unter Aufsicht von erfahrenem und ausgebildetem Personal
Die Einsatzkräfte, die ihn verwenden, müssen die körperliche Leistungsfähigkeit und eine gute Muskelkoordination besitzen. Die Fähigkeiten des Personals müssen vor Festle-
gung der Aufgabenverteilung beim Einsatz des Geräts geprüft werden. Die Rettungskräfte müssen in der Lage sein, dem Patienten im Bedarfsfall beistehen zu können.
2.5.1 ANWENDERAUSBILDUNG · Unabhängig von den in Vergangenheit mit ähnlichen Geräten erworbenen Erfahrungen muss der Inhalt dieses Handbuchs aufmerksam gelesen und auch verstanden wer-
den, bevor das Produkt zusammengebaut und einsatzbereit gemacht wird oder Wartungsarbeiten an ihm vorgenommen werden. Bei Zweifel wenden Sie sich für weitere Erläuterungen an Spencer Italia S.r.l. · Das Produkt darf nur von Personal angewendet werden, das im Gebrauch dieses und nicht eines anderen, ähnlichen Produkts geschult ist. · Die Eignung der Anwender für den Gebrauch des Produkts kann durch die Eintragung der Schulung bescheinigt werden, in der die geschulten Personen, die Ausbilder sowie Datum und Ort angegeben sind. Diese Dokumentation muss für mindestens 10 Jahre nach dem Lebensende des Produkts aufbewahrt werden und muss den zuständigen Behörden und/oder dem Hersteller auf Anfrage zur Verfügung gestellt werden. Geschieht dies nicht, werden von den zuständigen Stellen entsprechende Sanktionen erhoben.
· Nicht geschulte Personen dürfen während des Gebrauchs des Produkts keine Hilfe leisten, da dies zu Verletzungen an ihnen selbst oder an anderen führen könnte.
Hinweis: Spencer Italia S.r.l. steht immer zur Durchführung von Ausbildungskursen zur Verfügung.
2.5.2 AUSBILDUNG INSTALLATEUR Es ist keine Installation vorgesehen.
3. BEZUGSRICHTLINIEN
Der Händler oder Endanwender der von Spencer Italia S.r.l. hergestellten und/oder vermarkteten Produkte ist verpflichtet die im Bestimmungsland der Waren geltenden gesetzlichen Bestimmungen zu kennen, die auf die zu liefernden Geräte anwendbar sind (darunter die Vorschriften zu den technischen Angaben und/oder Sicherheitsanforderungen), und muss daher die Anforderungen kennen, die für die Übereinstimmung der betreffenden Produkte mit den gesetzlichen Bestimmungen des Landes benötigt werden.
BEZUG
TITEL DES DOKUMENTS
Verordnung EU 2017/745
EU-Verordnung zu medizinischen Geräten
NO SV SR LV ZH JA
4. EINLEITUNG
4.1 GEBRAUCH DES HANDBUCHS
Dieses Handbuch hat den Zweck, dem Notfallsanitäter die Informationen zu liefern, die für einen sicheren und bestimmungsgemäßen Gebrauch und für eine angemessene Wartung des Geräts benötigt werden. Hinweis: Das Handbuch ist fester Bestandteil des Geräts. Es muss daher für die gesamte Lebensdauer aufbewahrt werden und muss dem Gerät bei etwaigem Wechsel des Bestimmungsortes oder des Eigentümers beiliegen. Falls Gebrauchsanweisungen vorliegen, die sich auf ein Produkt beziehen, das von dem gelieferten abweicht, muss sich vor der Anwendung sofort an den Hersteller gewendet werden. . Die Benutzerhandbücher der Produkte von Spencer können von der Internetseite http://support.spencer.it heruntergeladen werden, oder man wendet sich an den Hersteller. Ausgenommen sind Artikel, deren Eigenart und vernunftmäßig vorhersehbarer Gebrauch zusätzlich zu den folgenden Warnhinweisen und Hinweisen auf dem Typenschild keine Benutzeranleitung erforderlich machen.
Unabhängig von den in Vergangenheit mit ähnlichen Geräten erworbenen Erfahrungen sollte dieses Handbuchs aufmerksam gelesen und auch verstanden werden, bevor das Produkt zusammengebaut und einsatzbereit gemacht wird oder Wartungsarbeiten an ihm vorgenommen werden.
4.2 TYPENSCHILDER UND RÜCKVERFOLGBARKEIT DES PRODUKTS
Jedes Produkt ist mit einem Typenschild versehen, das sich am Gerät und/oder an der Verpackung befindet, auf dem die Kennzeichnungsdaten der Herstellers, des Produkts, die CE-Kennzeichnung, die Seriennummer (SN) oder die Losnummer (LOT) angegeben ist. Dieses Schild darf niemals entfernt oder abgedeckt werden. Bei Beschädigung oder einer Abnahme kann beim Hersteller um ein Duplikat angefragt werden, da ansonsten die Gültigkeit der Garantie verfällt, da das Gerät nicht mehr rückverfolgbar ist. Falls die zugewiesene Losnummer/SN nicht mehr feststellbar ist, muss das Gerät überholt werden, wozu nur der Herstellers verantwortlich ist.
Die Verordnung EU 2017/754 verpflichtet die Hersteller und die Händler von medizinischen Geräten, deren Standort aufzuzeichnen. Wenn das Gerät sich an einem Sitz befindet, der von der Lieferadresse abweicht, oder es verkauft, verschenkt, verloren, gestohlen, exportiert oder zerstört, dauerhaft außer Gebrauch genommen wurde, oder wenn das Gerät nicht direkt von Spencer Italia S.r.l. geliefert wurde, muss es unter der Internetadresse http://service.spencer.it registriert werden, oder der Kundendienst (vgl. § 4.4) ist zu benachrichtigen.
18
4.3 SYMBOLE Symbol Bedeutung Gerät in Übereinstimmung mit der EU-Verordnung 2017/745 Medizinisches Gerät Hersteller Herstellungsdatum Unique Device Identifier
(01)08057711230006 (11) 200626 (10) 1234567890
Symbol
Bedeutung
Gefahr – Weist auf eine Gefahrensituation hin, die direkt zu schweren oder tödlichen Verletzungen führen kann.
Im Handbuch nachsehen
Losnummer
Produktcode
Achtung! Nach Bundesgesetz darf dieses Gerät nur von einem zugelassenen Arzt oder auf dessen Anordnung hin verkauft werden (nur für den US-Markt)
Kennzeichnung der Produktion Alphanumerischer Code, der die Produktionseinheit des Geräts kennzeichnet. Er setzt sich zusammen aus:
(01)0805771123 000
6 (11)200626 (10) 1234567890
Vorwahl des Unternehmens fortlaufende GS1
Prüfnummer Herstellungsdatum (JJMMTT) Losnummer/SN
4.4 GARANTIE UND KUNDENDIENST
Spencer Italia S.r.l. garantiert, dass die Produkte für die Dauer von einem Jahr ab Kaufdatum ohne Defekte sind.
Für Informationen zur richtigen Auslegung der Anweisungen, des Gebrauchs, Wartung, Installation und Zustellung wenden Sie sich bitte an den Kundendienst von Spencer Tel. +39 0521 541154, Fax +39 0521 541222, E-Mail [email protected]. Um den Kundendienstservice zu vereinfachen, bitte immer die Losnummer (LOT) oder Seriennummer (SN) angeben, die auf dem Typenschild auf der Verpackung oder dem Gerät angebracht ist. Die Garantie- sowie Kundendienstbedingungen sind auf der Internetseite http://support.spencer.it einsehbar. Hinweis: Vermerken und mit diesen Anweisungen aufbewahren: Los- (LOT) oder Seriennummer (SN), falls vorhanden, Ort und Datum des Kaufs, Datum des ersten Gebrauchs, Prüfdatum, Benutzername und Kommentare.
IT EN DE FR ES PT EL RO
5. WARNUNGEN/GEFAHREN
Warnungen, Gefahren, Hinweise und weitere wichtige Sicherheitsinformationen sind in diesem Abschnitt angegeben und im ganzen Handbuch deutlich sichtbar gemacht. Mindestens alle 6 Monate muss überprüft werden, ob aktualisierte Anweisungen und ihr Produkt betreffende Änderungen vorliegen. Diese Informationen sind frei auf der Internetseite www.spencer.it auf der betreffenden Produktseite einsehbar.
Gebrauchsweise des Produkts
Jeder Gebrauch des Produkts, der von dem in diesem Benutzerhandbuch beschriebenen abweicht, ist verboten.
Vor jedem Gebrauch ist immer zu überprüfen, dass das Produkt unbeschädigt ist, wie im Benutzerhandbuch angegeben, und bei Anomalien/Beschädigungen, die die Verwendbarkeit/Sicherheit beeinträchtigen können, muss es sofort außer Dienst genommen und der Hersteller benachrichtigt werden.
Das Produkt darf ohne Genehmigung des Herstellers nicht verfälscht und verändert werden (Änderungen, Anpassungen, Hinzufügungen, Reparaturen), da daraus Verletzungsgefahren für Personen sowie Materialschäden entstehen können. Andernfalls wird keinerlei Haftung für den nicht korrekten Einsatz oder für Schäden übernommen, die durch das Produkt selbst verursacht werden; ferner verfallen die CE-Kennzeichnung und die Produktgarantie Sicherstellen, dass alle Vorsichtsmaßnahmen getroffen wurden, um Gefahren durch Kontakt mit Blut oder Körpersekreten zu verhindern, sofern dies möglich ist. · Bei einem festgestellten Produktdefekt sofort ein gleichartiges Gerät benutzen, um die laufende Verwendung aufrechtzuerhalten. Das nicht mehr einsatztaugliche Gerät muss außer Gebrauch genommen werden. · Beim Gebrauch der Geräte sind sie so zu positionieren und zu einzustellen, dass sie die Arbeiten der Anwender und der Einsatz etwaiger anderer Geräte nicht behindern. · Den Kontakt mit scharfen oder scheuernden Gegenständen vermeiden. · Einsatztemperatur: von -5°C bis +50°C.
Lagerung · Das Produkt darf weder Verbrennungshitze und entzündbaren Stoffen ausgesetzt noch darf es mit ihnen in Kontakt kommen, sondern muss an einem trockenen, kühlen und
vor Licht und Sonneneinstrahlung geschütztem Ort gelagert werden. · Das Gerät nicht unter anderen mehr oder weniger schweren Materialien lagern, die es beschädigen können. · Das Produkt in seiner Originalverpackung lagern und transportieren, da ansonsten die Garantie verfällt. · Lagertemperatur: von -10°C bis +60°C .
Regulatorische Anforderungen
Der Händler oder Endanwender der von Spencer Italia S.r.l. hergestellten und/oder vermarkteten Produkte ist verpflichtet die im Bestimmungsland der Waren geltenden gesetzlichen Bestimmungen zu kennen, die auf die zu liefernden Geräte anwendbar sind (darunter die Vorschriften zu den technischen Angaben und/oder Sicherheitsanforderungen), und muss daher die Anforderungen kennen, die für die Übereinstimmung der betreffenden Produkte mit den gesetzlichen Bestimmungen des Landes benötigt werden.
· Spencer Italia S.r.l. ist umgehend und genau zu informieren (bereits bei Anfrage eines Kostenvoranschlags), wenn vom Hersteller etwaige Anforderungen eingehalten werden müssen, die für die Übereinstimmung der Produkte mit spezifischen gesetzlichen Bestimmungen des Gebiets erforderlich sind (darunter solche, die durch Verordnungen und/oder gesetzlichen Bestimmungen anderer Art herrühren).
· Mit der gebührenden Sorgfalt und Gewissenhaftigkeit dazu beitragen, dass die allgemeinen Sicherheitsanforderungen an die in Verkehr gebrachten Produkte eingehalten werden, indem den Endbenutzern alle Informationen zur Verfügung gestellt werden, die zur Durchführung der regelmäßigen Überprüfung der gelieferten Produkte erforderlich sind, genau wie im Benutzerhandbuch angegeben.
· Teilnahme an der Sicherheitsprüfung des in Verkehr gebrachten Produkts, indem die Informationen zu den Produktrisiken dem Hersteller sowie den Behörden, in deren Zuständigkeit die Handlungen liegen, übermittelt werden.
· Unbeschadet des Gesagten übernimmt der Händler oder Endbenutzer von nun an die weitest gehende Haftung im Zusammenhang mit der Nichteinhaltung der oben genannten Verpflichtungen und verpflichtet sich daher, Spencer Italia S.r.l. schadlos zu halten und/oder von allen nachteiligen Auswirkungen freizustellen.
· Unter Verweis auf die EU-Verordnung 2017/745 wird daran erinnert, dass öffentliche oder private Anwender, die bei Durchführung ihrer Tätigkeiten einen Unfall feststellen, an dem ein medizinisches Produkt beteiligt ist, außer dem Hersteller innerhalb der durch ein oder mehrere Ministerialerlasse festgelegten Fristen und Modalitäten dem Gesundheitsministerium Mitteilung machen müssen. Angestellte öffentlicher oder privater Gesundheitsdienste müssen den Hersteller über alle anderen Störungen informieren, die es ermöglichen, Maßnahmen zum Schutz und zur Sicherstellung der Gesundheit von Patienten und Anwendern zu ergreifen.
CS BG DA FI NL NO SV SR LV ZH JA
19
IT EN DE FR ES PT EL RO CS BG DA FI
Allgemeine Hinweise zu medizinischen Geräten
Der Anwender muss aufmerksam neben den allgemeinen auch die nachfolgend aufgeführten Hinweise lesen.
· Es ist nicht vorgesehen, dass die Anwendung des Geräts länger dauert als die Zeit, die für die ersten Maßnahmen und den anschließenden Transport zur nächstgelegenen Rettungsstelle erforderlich ist.
Das Gerät nicht benutzen, wenn an ihm oder Teilen von ihm Löcher, Abrisse, Ausfransungen oder übermäßiger Verschleiß bemerkt werden. Das Gerät nicht absichtlich verfälschen oder abändern. Die Änderung könnte ein unvorhergesehenes Nutzungsverhalten verursachen und den Patienten oder das Rettungspersonal schädigen und würde die Garantie verfallen lassen und den Hersteller von allen Haftungen entbinden. · Während des Gebrauchs des Geräts muss die Beihilfe von Fachpersonal sichergestellt sein und es müssen mindestens zwei Rettungshelfer zugegen sein. · Die durch Ihre Organisation erlassenen internen Verfahren und Protokolle anwenden. · Desinfizierungen müssen gemäß den validierten Zyklusparametern durchgeführt werden, die in den spezifischen technischen Normen angegeben sind. · Keine Trocknungsgeräte zur Trocknung des Geräts verwenden. · Bei freiliegender und/oder verletzter Haut sind die mit dem Patienten in Kontakt stehenden Flächen mit einem OP-Tuch abzudecken, das den Biokompatibilitätsvorschriften entspricht, um die Gesundheit des Patienten zu schützen.
6. SPEZIFISCHE HINWEISE
Vor der Nutzung der Integral-Haltegurte müssen auch sorgfältig alle Angaben in diesem Benutzerhandbuch gelesen, verstanden und befolgt werden.
· Immer die Positionsangaben beachten, die von dem Gerät vorgegeben sind, mit dem die Gurte benutzt werden. Zudem muss der Anwender berücksichtigen, dass die Maße des Patienten nicht die Verwendbarkeit des Produkts beeinträchtigt.
· Immer die Anzahl an Gurten anbringen, die von der verwendeten Transporteinrichtung vorgesehen sind. · Unter Angaben eines zuständigen Beschäftigten sind ein Wartungsprogramm und regelmäßige Prüfungen zu bestimmen. Die Person, der die ordentliche Wartung des Geräts
anvertraut ist, muss die vom Hersteller vorgesehenen Grundanforderungen im Rahmen dieser Gebrauchsanweisungen sicherstellen. · Alle Wartungstätigkeiten müssen eingetragen und mit den entsprechenden technischen Tätigkeitsberichten dokumentiert werden. Die Dokumentation muss für mindestens
10 Jahre ab Lebensende des Geräts aufbewahrt werden und muss auf Anfrage den zuständigen Behörden und/oder dem Hersteller zur Verfügung gestellt werden.
Mit den Gurten, die am für den Einsatz vorgesehenen Produkt angebracht sind, Rettungssimulationen und einer den Patienten simulierenden Last und Zubehör durchzuführen. Vor jedem Gebrauch ist immer die Unversehrtheit des Geräts und seiner Komponenten zu überprüfen, wie im Benutzerhandbuch ausgewiesen. Bei Anomalien oder Schäden, die die Verwendbarkeit und die Sicherheit des Geräts und somit des Patienten und der Einsatzkraft gefährden können, darf das Gerät nicht mehr benutzt werden. Die vom Medizinischen Notfalldienst genehmigten Verfahren für die Positionierung und den Patiententransport befolgen. · Den Kontakt mit scharfen Gegenständen vermeiden. · Die vom Medizinischen Notfalldienst genehmigten Verfahren für die Ruhigstellung und den Patiententransport befolgen. · Um die Lebensdauer des Geräts zu bewahren, muss es möglichst vor UV-Strahlen und widrigen Wetterverhältnissen geschützt werden. · Sicherstellen, dass das Gurtschloss fest am Gurt befestigt, unversehrt und einsatzbereit sind.
7. RESTRISIKO Restrisiken sind nicht gegeben, also Risiken, die sich trotz Einhaltung aller Hinweise dieses Benutzerhandbuchs ereignen könnten.
8. TECHNISCHE DATEN UND KOMPONENTEN Hinweis: Spencer Italia S.r.l. behält sich das Recht vor, ohne Vorankündigung Änderungen anzubringen. .
BESCHREIBUNG
1 Karabinerhaken für Stifte (falls vorhanden)
2 Querbänder mit Strap
3 Längsband
NL
4 V-Bänder
NO SV
Bänder Nr. Befestigungsart Material Gewicht
ROCK STRAPS 10
Strap
Polypropylen/Nylon 600g
T-STRAPS 10
Strap
Polypropylen/Nylon 800g
REFLEX STRAPS 10
Strap
Polypropylen/Nylon 600g
PIN STRAPS
10
Strap+Karabinerhaken aus Metall
Polypropylen/Nylon/ Metalllegierung
1500g
ECS STRAPS 12
Strap
Polypropylen/Nylon 800g
RSP STRAPS 10
Strap
Polypropylen/Nylon 350g
SR LV ZH JA
9. INBETRIEBNAHME
Für den Erstgebrauch überprüfen, dass:
· Die Verpackung unversehrt ist und das Gerät während des Transports geschützt war · Überprüfen, dass alle Teile der Lieferliste vorhanden sind. · Allgemeine Betriebseignung des Geräts · Reinigungszustand des Produkts · An der ganzen Vorrichtung keine Anzeichen von Schnitten, Löchern, Rissen oder Abschürfungen · Verschleißgrad der Vorrichtung. · Die korrekte Funktion der Karabinerhaken überprüfen, falls im Modell vorhanden · Überprüfen, dass die Karabinerhaken, sofern sie beim Modell vorhanden sind, einsatztauglich sind · Die korrekte Haftung der Strapseinlagen prüfen .
Im Absatz 11 die Gebrauchsweisen für den Ablauf der oben genannten Überprüfen kontrollieren. Das Gerät unter keinen Umständen in seinen Teilen verändern, da dies zu Schäden am Patienten und/oder am Rettungspersonal führen kann. .
Werden die oben genannten Maßnahmen unterlassen, ist die Sicherheit beim Gebrauch des Geräts nicht gegeben, woraus sich ein Schadensrisiko für den Patienten, die Einsatzkräfte und das Gerät selbst ergeben kann. Für spätere Anwendungen die unter Absatz 12 angegebenen Maßnahmen ausführen.
20
Wenn die oben genannten Bedingungen erfüllt sind, kann das Gerät als betriebsbereit betrachtet werden. Andernfalls muss es sofort außer Betrieb genommen und der Hersteller kontaktiert werden.
10. ANWENDUNGSEIGENSCHAFTEN
Für die Anwendungseigenschaften siehe Absatz 11 – Gebrauchsweise.
11. GEBRAUCHSWEISE
Vor der Behandlung des Patienten müssen primäre medizinische Untersuchungen durchgeführt werden. Vor der Nutzung gleich welcher in diesem Handbuch beschriebenen Art von Gurt aufmerksam die Benutzeranweisung des Geräts durchlesen, mit dem der Gurt eingesetzt werden soll.
11.1 ANWENDUNG DER GURTE
Befolgen Sie die vom zuständigen Rettungsdienst genehmigten Verfahren zur Immobilisierung, Positionierung und zum Transport von Patienten. Die folgenden Verfahren sind auf der Grundlage allgemeiner Nutzungsinformationen geschrieben. 1. Der Patient wird auf einem Wirbelsäulenbrett mit einer Halskrause gelagert 2. Legen Sie den Gurt unter Aufrechterhaltung einer angemessenen Immobilisierung am Patienten an, wobei die V-Bänder etwa 2/3 cm unterhalb des Halskragens angeordnet
werden 3. Positionieren Sie die anderen Querbänder auf diese Weise: · der Brustgurt in Brusthöhe knapp unterhalb der Schultern · der Beckengurt in Höhe der Beckenkämme · das erste Beingurt am Oberschenkel, in der Nähe des Knies · das zweite Beingurt an den Schienbeinen, in der Nähe der Knöchel (wenn der Pflegebedürftige klein ist, rollen Sie die Gurten auf) Achten Sie immer auf die Bereiche, die möglicherweise ein Trauma und/oder Frakturen erlitten haben.
4. Legen Sie ggf. Kopfstützen und/oder Fußfesseln an. 5. ausgehend von den Schultern in Richtung der Füße die Gurte gleichzeitig in die entsprechenden Löcher auf beiden Seiten der Wirbelsäule einführen und dabei die Karabinerhaken verwenden, die, falls vorhanden, an den Stiften des Wirbelsäulenbretts eingehängt werden müssen. 6. Befestigen Sie die Gurte mit gleichmäßigem Zug auf beiden Seiten, von den Schultern bis zu den Füßen, und achten Sie auf mögliche Atemwegs- und Bauchbeschwerden; 7. Stellen Sie sicher, dass der Patient ausreichend immobilisiert ist, und setzen Sie dann die Manöver gemäß den Richtlinien des jeweiligen Rettungsdienstes fort.
Der RSP-Pädiatriegurt, der für die Verwendung mit dem Baby Go Wirbelsäulenbrett vorgesehen ist, ist mit einem Maßband mit farbigen Bereichen ausgestattet, die eine schnellere Identifizierung der Seite ermöglichen, die in Bezug auf die Körpergröße des Patienten am ehesten geeignet ist. Für die Auswahl des Gerätes und dessen korrekte Anwendung ist jedoch allein der Retter verantwortlich.
12. REINIGUNG UND WARTUNG
Spencer Italia S.r.l. lehnt jede Haftung für direkte oder indirekte Schäden ab, die auf die unsachgemäße Verwendung des Produkts und der Ersatzteile und / oder in jedem Fall auf Reparaturarbeiten zurückzuführen sind, die von einer anderen Person als dem Hersteller durchgeführt werden, der interne und externe Techniker einsetzt, die fachlich ausgebildet und dazu befugt sind. Darüber hinaus erlischt die Garantie.
· Während aller Kontroll-, Wartungs- und Hygienemaßnahmen muss der Bediener geeignete persönliche Schutzausrüstung wie Handschuhe, Schutzbrille usw. tragen. · Es ist ein Wartungsprogramm, regelmäßige Überprüfungen und eine Verlängerung der durchschnittlichen Lebensdauer, sofern dies vom Hersteller im Benutzerhandbuch
angegeben ist, festzulegen, indem eine Bezugsperson angegeben wird, die die im Handbuch bestimmten Grundanforderungen erfüllt. · Die Häufigkeit der Kontrollen richtet sich nach Faktoren, wie die gesetzlichen Bestimmungen, die Art des Gebrauchs, die Häufigkeit des Gebrauchs, die Umweltbedin-
gungen während der Verwendung und die Lagerung. · Die Reparatur der von Spencer Italia S.r.l. hergestellten Produkte muss vom Hersteller durchgeführt werden, der interne und externe Fachleute einsetzt, die Originalersa-
tzteile benutzen und eine qualitativ hochwertige Reparatur bieten, die streng den technischen Angaben entsprich, die vom Hersteller vorgegeben werden. Spencer Italia S.r.l. lehnt jede Haftung für direkte oder indirekte Schäden ab, die auf die unsachgemäße Verwendung der Ersatzteile und / oder auf Reparaturarbeiten zurückzuführen sind, die von nicht befugtem Personal ausgeführt wurden. · Die Überholung, also Arbeiten, die zur Wiederherstellung der technischen und funktionalen Sicherheit des benutzten Geräts dienen, Beispiel erneuerte Zulassung, müssen vom Hersteller ausgeführt werden. · Alle Wartungs- und Überarbeitungstätigkeiten müssen eingetragen und mit den entsprechenden technischen Tätigkeitsberichten dokumentiert werden. Die Dokumentation muss für mindestens 10 Jahre ab Lebensende des Produkts aufbewahrt werden und muss auf Anfrage den zuständigen Behörden und/oder dem Hersteller zur Verfügung gestellt werden. · Die für wiederverwendbare Produkte vorgesehene Reinigung muss unter Einhaltung der vom Hersteller im Benutzerhandbuch gemachten Angaben erfolgen, um die Gefahr von Kreuzinfektionen aufgrund von Sekreten und/oder Rückständen zu vermeiden.
12.1 REINIGUNG
Wird das Produkt nicht gereinigt besteht die Gefahr von Kreuzinfektionen durch Sekrete und/oder Rückständen. Während aller Kontroll- und Hygienemaßnahmen muss der Bediener geeignete persönliche Schutzausrüstung wie Handschuhe, Schutzbrille usw. tragen.
Alle Metallteile, die äußeren Einflüssen ausgesetzt sind, werden Oberflächenbehandlungen und/oder Lackierungen unterzogen, um eine bessere Beständigkeit zu erzielen. Die ausgesetzten Teile mit lauwarmem Wasser und neutraler Seife waschen; niemals Lösungsmittel oder Fleckentferner verwenden. Sorgfältig mit lauwarmem Wasser nachspülen und überprüfen, dass alle Seifenreste entfernt wurden, die das Produkt verschleißen oder beschädigen und seine Lebensdauer verringern könnte. Vermeiden Sie die Verwendung von Hochdruckwasser. Vor dem Zusammensetzung vollständig trocknen lassen. Die Trocknung nach dem Waschen oder nach dem Einsatz in feuchter Umgebung muss natürlich und nicht erzwungen erfolgen; keine Flammen oder direkte Wärmequellen benutzen. Zur Desinfektion Produkte verwenden, die nicht nur als medizinische chirurgische Hilfsmittel eingestuft sind, sondern auch keine lösungsmittel- oder ätzenden Wirkungen auf die Materialien haben, aus denen das Gerät besteht. Alle Vorsichtsmaßnahmen ergreifen, um sicherzustellen, dass kein Risiko einer Kreuzinfektion oder Kontamination von Patienten und Einsatzkräften besteht. Für Einwegprodukte ist keine Reinigung vorgesehen, sofern das Produkt gemäß den Vorschriften des Herstellers gelagert und verpackt ist.
12.2 ORDENTLICHE WARTUNG
You must establish a program for periodic checks, identifying a designated reference person. The person entrusted with device maintenance must ensure the basic Ein beauftragter Beschäftigter muss regelmäßige Prüfungen festlegen. Die Person, der die Wartung des Geräts anvertraut ist, muss die Grundanforderungen im Rahmen dieser Gebrauchsanweisungen erfüllen. Alle Wartungsarbeiten müssen eingetragen und durch die technischen Tätigkeitsberichte dokumentiert werden. Diese Dokumentation muss für mindestens 10 Jahre nach dem Lebensende des Geräts aufbewahrt werden und muss den zuständigen Behörden und/oder dem Hersteller auf Anfrage zur Verfügung gestellt werden.
Während aller Kontroll-, Wartungs- und Hygienemaßnahmen muss der Bediener geeignete persönliche Schutzausrüstung wie Handschuhe, Schutzbrille usw. tragen.
Das Gerät erfordert kein Programm für eine ordentliche Wartung, jedoch müssen Kontrollen vorgenommen werden, um zu überprüfen: · Allgemeine Betriebseignung des Geräts · Reinigungszustand des Geräts (zur Erinnerung: wird das Gerät nicht gereinigt, kann dies zur Kreuzinfektionen führen) · Erfüllung der vom Benutzerhandbuch im Abschnitt 5 Hinweise und 6 Spezifische Hinweise vorgesehenen Anforderungen · Erfüllung der vom Benutzerhandbuch im Abschnitt 11 Gebrauchsweise vorgesehenen Anforderungen
IT EN DE FR ES PT EL RO CS BG DA FI NL NO SV SR LV ZH JA
21
IT EN DE FR ES PT EL RO CS BG
Nur Komponenten/Ersatzteile und/oder originale oder von Spencer Italia S.r.l. genehmigte Zubehörteile verwenden, damit jeder Vorgang durchgeführt wird, ohne dass es zu Umbauten oder Änderungen am Gerät kommt. Andernfalls wird keinerlei Haftung für den nicht korrekten Einsatz oder für etwaige Schäden durch das Gerät am Patienten oder an der Einsatzkraft übernommen da die Garantie sowie die Übereinstimmung mit der EU-Verordnung 2017/745 aufgehoben ist.
12.3 REGELMÄSSIGE REVISION Für das Gerät ist keine regelmäßige Revision vorgesehen. 12.4 AUSSERORDENTLICHE WARTUNG
Die außerordentliche Wartung darf nur vom Hersteller ausgeführt werden, der interne und externe Techniker einsetzt, die fachlich ausgebildet und von ihm dazu befugt sind.
Für Spencer Italia S.r.l. sind nur Wartungen gültig, die von spezialisierten und vom Hersteller befugten Technikern ausgeführt werden. 12.5 LEBENSDAUER
Das Gerät hat, wenn es nach den nachfolgenden Anweisungen benutzt wird, eine Lebensdauer von 5 Jahren ab Kaufdatum.
Spencer Italia S.r.l. übernimmt keinerlei Haftung für den nicht korrekten Einsatz oder für etwaige Schäden durch das Gerät, das die zulässige maximale Lebensdauer überschritten hat.
13. SCHADENSTABELLE
PROBLEM
URSACHE
ABHILFE
Der Karabinerhaken kann nicht am Stift des Wirbelsäulenbretts befestigt werden
Der Karabinerhaken ist beschädigt oder die Öffnung wird durch Frem-
dkörper blockiert
Prüfen Sie, ob die Öffnung durch nichts behindert wird. Wenn alles sauber ist und das Problem nicht behoben wurde, nehmen Sie das Gerät sofort außer Betrieb und wenden Sie sich an den Hersteller
Der Gurt schließt nicht
Strapsbereiche verschmutzt oder abgelöst
Reinigen Sie die Strapsbereiche und prüfen Sie die korrekte Haftung. Wenn das Problem weiterhin besteht, nehmen Sie das Gerät außer Betrieb und wenden Sie sich an den Hersteller
Falls das Problem oder der Schaden nicht in der obigen Liste enthalten ist, wenden Sie sich bitte an den Kundendienst von Spencer Italia S.r.l.
14. ZUBEHÖR Es sind keine Zubehörteile für diese Vorrichtungen vorhanden.
15. ERSATZTEILE Es sind keine Ersatzteile für diese Vorrichtungen vorhanden.
16. ENTSORGUNG Sobald die Geräte und ihr Zubehör unbrauchbar sind und nicht durch bestimmte Stoffe kontaminiert wurden, können sie als normaler fester Haushaltsabfall entsorgt werden. Andernfalls müssen die geltenden Vorschriften zur Entsorgung eingehalten werden.
DA
FI
NL
NO
SV
SR
LV
ZH JA
Hinweis
Die in diesem Dokument enthaltenen Informationen können ohne Vorankündigung geändert werden und stellen eine Verpflichtung der Spencer Italia S.r.l. dar, die Änderungen unterworfen ist. Die Bilder sind Beispiele und können von den eigentlichen Bildern des Geräts abweichen.
© Copyright Spencer Italia S.r.l. Alle Rechte vorbehalten. Kein Teil des Dokuments darf ohne die vorherige schriftliche Zustimmung von Spencer Italia S.r.l. fotokopiert, nachgedruckt oder in eine andere
Sprache übersetzt werden.
22
1. MODÈLES Les modèles de base reportés ci-dessous peuvent être sujets à des améliorations ou des modifications sans préavis.
· T-Straps
· Pin Straps
· Reflex Straps
· ECS Straps
· Rock Straps
· RSP Straps
2. UTILISATION
2.1 UTILISATION ET BÉNÉFICES CLINIQUES
Les sangles araignées sont des dispositifs qui aident à immobiliser le patient sur les plans durs Spencer.
2.2 PATIENTS DESTINATAIRES
Aucune indication particulière liée au groupe de patients n’est indiquée. La conformation du produit permet son utilisation sur n’importe quelle personne, dans les limites imposées par les dimensions du dispositif. S’il fallait transporter des enfants, ce sera aux secouristes d’établir si les systèmes de sangles sont appropriés à son immobilisation ou si au contraire, il faudra utiliser un autre dispositif.
2.3 CRITÈRES DE SÉLECTION DES PATIENTS
Les critères de sélection des patients attendus sont ceux applicables au dispositif avec lesquels la ceinture est utilisée.
2.4 CONTRE-INDICATIONS ET EFFETS COLLATÉRAUX INDÉSIRABLES Aucune contre-indication particulière ou aucun effet indésirable dérivant de l’utilisation du dispositif n’est connu, du moment qu’il est utilisé comme décrit dans le manuel d’utilisation.
2.5 UTILISATEURS ET INSTALLATEURS
Les utilisateurs prévus sont des personnes préposées au secours, experts dans le déplacement, l’immobilisation et le transport du patient. Les dispositifs ne doivent pas être utilisés par des utilisateurs profanes.
Les sangles araignées sont un dispositif destiné uniquement à une utilisation professionnelle. Ne jamais autoriser des personnes non formées à aider pendant l’utilisation du produit, puisqu’elles pourraient provoquer des blessures à eux-mêmes ou à d’autres personnes. Malgré tous les efforts, les tests en laboratoires, les essais, les certifications de bon fonctionnement, les instructions d’utilisation, les normes ne réussissent pas toujours à reproduire la pratique; les résultats obtenus dans les conditions réelles d’utilisation du produit dans l’environnement naturel peuvent donc différer certaines fois de manière importante. Les meilleures instructions sont la pratique continue d’utilisation sous la supervision de personnel compétent et préparé. Les opérateurs qui les utilisent doivent posséder la capacité physique à utiliser le dispositif et avoir une bonne coordination musculaire. Les capacités des opérateurs doivent être évaluées avant la définition des rôles dans l’utilisation du dispositif.
Les opérateurs doivent être capables de fournir l’assistance nécessaire au patient.
2.5.1 FORMATION DES UTILISATEURS · Indépendamment du niveau d’expérience acquis par le passé avec des dispositifs analogues, il faut lire attentivement et comprendre le contenu du présent manuel avant
l’installation, l’utilisation du produit ou toute intervention d’entretien. En cas de doutes, contacter Spencer Italia S.r.l. pour obtenir les éclaircissements nécessaires. · Le produit doit être utilisé uniquement par du personnel formé à l’utilisation de ce produit et non d’autres produits analogues. · La capacité des utilisateurs à utiliser le produit peut être attestée avec l’enregistrement de la formation, dans laquelle sont spécifiés les personnes formées, les formateurs, la
date et le lieu. Cette documentation doit être conservée au moins pendant 10ans après la fine de vie du produit et doit être mise à disposition des autorités compétentes et/ou du fabricant, si nécessaire. Si elle devait manquer, les organes préposés appliqueront les éventuelles sanctions prévues. · Ne jamais autoriser des personnes non formées à aider pendant l’utilisation du produit, puisqu’elles pourraient se procurer des lésions ou à d’autres personnes. Remarque: Spencer Italia S.r.l. est toujours à disposition pour proposer des cours de formation. .
2.5.2 FORMATION INSTALLATEUR
Aucune installation n’est prévue.
3. STANDARD DE RÉFÉRENCE
En qualité de distributeur ou d’utilisateur final des produits fabriqués et/ou commercialisés par Spencer Italia S.r.l., il est strictement demandé de connaître les dispositions de loi en vigueur dans le pays de destination de la marchandise, applicables aux dispositifs objet de la fourniture (y compris les normes relatives aux caractéristiques techniques et/ou aux exigences de sécurité) et, donc, de connaître les mesures nécessaires pour assurer la conformité de ces produits à toutes les exigences de loi du territoire.
RÉFÉRENCE
TITRE DU DOCUMENT
Réglementation UE 2017/745
Réglementation UE relative aux dispositifs médicaux
4. INTRODUCTION
4.1 UTILISATION DU MANUEL
Le présent manuel a pour but de fournir à l’opérateur sanitaire les informations nécessaires pour une utilisation sécurisée et appropriée et pour un entretien adéquat du dispositif.
Remarque: le manuel fait partie intégrante du dispositif; il doit donc être conservé pendant toute la durée de vie du dispositif et devra l’accompagner lors d’éventuels changements de destination ou de propriété. Si des instructions d’utilisation relatives à un autre produit devaient être présente, différent de celui reçu, contacter immédiatement le fabricant avec de l’utiliser. Les manuels d’utilisation des produits Spencer, peuvent être téléchargés depuis le site http://support.spencer.it ou en contactant le fabricant. À l’exception des articles dont le caractère essentiel et une utilisation raisonnable et prévisible sont tels de ne pas rendre nécessaire la rédaction d’instructions, en plus des avertissements suivants et des indications présentes sur l’étiquette.
Indépendamment du niveau d’expérience acquis par le passé avec des dispositifs analogues, il est recommandé de lire attentivement le présent manuel avant l’installation, l’utilisation du produit ou toute intervention d’entretien.
4.2 ÉTIQUETAGE ET CONTRÔLE DE LA TRAÇABILITÉ DU DISPOSITIF
Chaque dispositif est équipé d’une étiquette, placée sur le dispositif et/ou sur l’emballage, sur laquelle sont présentes les données d’identification du fabricant, du produit, du marquage CE, du numéro d’immatriculation (SN) ou de lot (LOT). L’étiquette ne doit jamais être retirée ou couverte. En cas d’endommagement ou de retrait, demander un duplicata au fabricant, sous peine de voir la validité de la garantie diminuée ou garantie, puisque le dispositif ne pourra plus être tracé. S’il devait être impossible à remonter au lot/SN attribué, il faut effectuer le reconditionnement du dispositif, prévu uniquement sous la responsabilité du fabricant.
La réglementation UE 2017/754 requiert aux producteurs et aux distributeurs de dispositifs médicaux de garder une trace de leur emplacement. Si le dispositif se trouve dans un lieu différent de l’adresse à laquelle il a été expédié ou a été vendu, donné, perdu, volé, exporté ou détruit, retiré de manière permanente à l’utilisation, ou bien si le dispositif n’a pas été livré directement par Spencer Italia S.r.l., enregistrer le dispositif à l’adresse http://service.spencer.it, ou bien informer l’assistance clients (voir § 4.4).
IT EN DE FR ES PT EL RO CS BG DA FI NL NO SV SR LV ZH JA
23
IT EN DE FR ES PT EL RO
4.3 SYMBOLES Symbole Sens Dispositif conforme à la réglementation UE 2017/745 Dispositif médical Fabricant Date de fabrication Unique Device Identifier
(01)08057711230006 (11) 200626 (10) 1234567890
Symbole Sens Danger Indique une situation de danger qui peut entraîner une situation directement liée à des lésions graves ou létales
Consulter le manuel d’utilisation
Numéro de lot
Code du produit
Attention: La loi fédérale restreint la vente de ce dispositif à un praticien agréé ou sur son ordre (uniquement pour le marché américain)
Identification de la production Code alphanumérique qui identifie les unités de production du dispositif, composé de:
(01)0805771123 000
6 (11)200626 (10) 1234567890
préfixe de l’entreprise progressif GS1
numéro de contrôle date de production (YYMMDD) numéro de lot/SN
4.4 GARANTIE ET ASSISTANCE Spencer Italia S.r.l. garantit que ses produits sont sans défaut pendant une période d’un an à partir de la date de l’achat.
Pour toute information relative à l’interprétation correcte des instructions, à l’utilisation, à l’entretien, à l’installation ou au retour, contacter le service assistance client Spencer tél. +39 0521 541154, fax +39 0521 541222, e-maill [email protected]. Pour faciliter les opérations d’assistance, toujours indiquer le numéro du lot (LOT) ou de série (SN) qui se trouvent sur l’étiquette appliquée à l’emballage ou directement sur le dispositif. Les conditions de garantie et d’assistance sont disponibles sur le site http://support.spencer.it.
Remarque: Enregistrer et conserver avec ces instructions: lot (LOT) ou numéro de série (SN) si présent, lieu et date d’achat, date de première utilisation, date des contrôles, nom des utilisateurs et commentaires.
CS BG DA FI NL NO SV SR LV ZH JA
5. AVERTISSEMENTS/DANGERS
Les avertissements, les dangers, les remarques et toute autre information de sécurité importante sont indiqués dans cette section et clairement visibles sur tout le manuel. Au moins tous les 6mois, il est important de vérifier la présence d’instructions actualisées et les éventuelles modifications qui concernent le produit. Ces informations peuvent être librement consultées sur le site www.spencer.it sur la page dédiée au produit.
Fonctionnement du produit
Il est interdit d’utiliser le produit pour toute autre utilisation différente que celle décrite dans le manuel d’utilisation.
Avant chaque utilisation, toujours vérifier l’intégrité du produit, comme spécifié dans le manuel d’utilisation; et en cas d’anomalies/dommages qui peuvent compromettre la fonctionnalité/sécurité, il faut immédiatement le retirer du service et contacter le fabricant.
Le produit ne doit subir aucune modification sans l’autorisation du fabricant (modification, retouche, ajout, réparation), puisqu’elles peuvent constituer des dangers imminents de blessure aux personnes ainsi que des dommages matériaux. Dans le cas contraire, l’entreprise décline toute responsabilité sur le fonctionnement incorrect ou sur les éventuels dommages provoqués par le produit; de plus, le marquage CE et la garantie du produit sont annulés. S’assurer d’avoir adopté toutes les précautions afin d’éviter les dangers dérivant du contact avec le sang ou les sécrétions corporelles, si applicable. · Si l’on remarque un dysfonctionnement du produit, le changer immédiatement par un dispositif analogue pour garantir la continuité des opérations en cours. Le dispositif non conforme doit être mis hors d’usage. · Pendant l’utilisation des dispositifs, les placer et les régler de manière à ne pas entraver les actions des opérateurs et l’utilisation d’autres appareils éventuels. · Éviter le contact avec des objets coupants ou abrasifs. · Température d’utilisation: de -5°C à + 50°C.
Stockage · Le produit ne doit pas être exposé ni entrer en contact avec des sources de chaleur de combustion et des agents inflammables, mais doit être stocké dans un lieu sec, frais,
protégé de la lumière et du soleil. · Ne pas stocker le produit sous d’autres matériaux plus ou moins lourds qui pourraient endommager le dispositif. · Stocker et transporter le produit dans son emballage original; dans le cas contraire, la garantir est annulée. · Température de stockage: de -10°C à +60°C.
Exigences régulatoires
En qualité de distributeur ou d’utilisateur final des produits fabriqués et/ou commercialisés par Spencer Italia S.r.l., il est strictement demandé de connaître les dispositions de loi en vigueur dans le pays de destination de la marchandise, applicables aux dispositifs objet de la fourniture (y compris les normes relatives aux caractéristiques techniques et/ou aux exigences de sécurité) et, donc, de connaître les mesures nécessaires pour assurer la conformité de ces produits à toutes les exigences de loi du territoire.
· Informer rapidement et de manière détaillée Spencer Italia S.r.l. (déjà en passe de demande de devis) sur les éventuelles mesures dépendantes du fabricant, nécessaires pour la conformité des produits aux exigences spécifiques de la loi du territoire (y compris celles dérivant des réglementations et/ou dispositifs normatifs de toute autre nature).
· Agir, avec le soin et la diligence nécessaire, pour contribuer à garantir la conformité aux exigences générales de sécurité des dispositifs distribués sur le marché, en fournissant aux utilisateurs finaux toutes les informations nécessaires pour le déroulement des activités de révision périodiques sur les dispositifs fournis, exactement comme indiqué dans le manuel d’utilisation.
· Participer au contrôle de sécurité du produit distribué sur le marché, en transmettant les informations concernant les disques du produit au fabricant ainsi qu’aux autorités compétentes pour les actions de compétence respectives.
· Une fois établi ce qui précède, le distributeur ou l’utilisateur final assume dès lors toute responsabilité plus ample liée au non-respect de ce qui est indiqué ci-dessus avec pour conséquence une obligation de garder indemne et/ou décharger Spencer Italia S.r.l. De tout éventuel effet préjudiciable relative.
· En référence à la réglementation UE 2017/745, il faut rappeler que les opérateurs publics ou privés, qui dans l’exercice de leur activité relèvent un incident qui impliquer un produit médical sont tenus de le communiquer au Ministère de la Santé, selon les termes et les modalités établies avec un ou plusieurs décrets ministériels, et au fabricant. Les opérateurs sanitaires publics ou privés sont tenus de communiquer au fabricant tout autre inconvénient qui puisse autoriser l’adoption des mesures capables de garantir la protection et la santé des patients et des utilisateurs.
24
Avertissements généraux pour les dispositifs médicaux
L’utilisateur doit également lire attentivement, en plus des avertissements généraux, ceux listés ci-dessous.
· Il n’est pas prévu que l’application du dispositif dure au-delà du temps nécessaire aux opérations des premiers soins et des phases suivantes de transport jusqu’au poste de secours de plus proche.
Ne pas utiliser le dispositif ou ses parties si ce dernier est troué, déchiré, effiloché ou excessivement usé. Ne pas altérer ou modifier de manière arbitraire le dispositif, la modification pourrait rendre son fonctionnement imprévisible et provoquer des dangers au patient ou aux secouristes et impliquerait l’annulation de la garantie et déchargerait le Fabricant de toute responsabilité. · Le dispositif doit être utilisé par du personnel qualifié et par au moins deux opérateurs. · Suivre les procédures et les protocoles internes approuvés par la propre organisation. · Les activités de désinfection doivent être exécutées selon les paramètres de cycle validé, rapportés dans les normes techniques spécifiques. · Ne pas utiliser de machines sécheuses pour sécher le dispositif. · Dans le cas de peau exposée et/ou blessée, couvrir la surface en contact avec le patient avec un drap chirurgical qui respecte les normes de biocompatibilité pour protéger la santé du patient.
6. AVERTISSEMENTS SPÉCIFIQUES
Pour l’utilisation des sangles araignées, il est également nécessaire d’avoir lu, compris et de suivre soigneusement toutes les indications présentes dans le manuel d’utilisation.
· Toujours respecter les instructions de positionnement déterminées par le dispositif avec lequel on utilise les sangles. De plus, l’opérateur doit évaluer que l’encombrement du patient ne réduit pas la fonctionnalité du produit.
· Toujours appliquer le nombre de ceintures prévu par le dispositif de transport utilisé. · Établir un programme d’entretien et de contrôles périodiques, en identifiant une personne de référence. Le sujet auquel est confié l’entretien ordinaire du dispositif doit
garantir les exigences de base prévues par le fabricant dans les présentes instructions d’utilisation. · Toutes les activités d’entretien doivent être enregistrées et documentées avec les rapports relatifs d’intervention technique; la documentation devra être conservée au
moins pendant 10ans à partir de la fin de vie du dispositif et devra être mise à disposition des autorités compétentes et/ou du fabricant, si nécessaire.
Effectuer des simulations de secours avec les sangles appliquées au produit avec lequel l’utilisation est prévue et une charge simulant un patient et des accessoires, avant la mise en service du dispositif. Avant chaque utilisation, toujours vérifier l’intégrité du dispositif et de ses composants, comme spécifié dans le manuel d’utilisation. En cas d’anomalies ou de dommages qui peuvent compromettre la fonctionnalité et la sécurité du dispositif, et donc du patient et de l’opérateur, il faut mettre hors de service le dispositif. Suivre les procédures approuvées par le service médical d’urgence pour le positionnement et le transport du patient. · Éviter le contact avec des objets coupants. · Suivre les procédures approuvées par le service médical d’urgence pour l’immobilisation et le transport du patient. · Pour préserver la durée de vie du dispositif, il faut le protéger le plus possible de rayons UV et des conditions météorologiques défavorables. · S’assurer que les boucles soient parfaitement ancrées dans la sangle, qu’elles soient en parfait état et qu’elles fonctionnent.
7. RISQUE RÉSIDUEL Aucun risque résiduel n’est identifié, c’est-à-dire des risques qui pourraient être créés, malgré le respect de tous les avertissements du présent manuel d’utilisation.
8. DONNÉES TECHNIQUES ET COMPOSANTS Remarque: Spencer Italia S.r.l. se réserve le droit d’apporter des modifications aux caractéristiques sans préavis.
DESCRIPTION
1 Mousquetons pour broche (si présents)
2 Sangles transversales avec strap
IT EN DE FR ES PT EL RO CS BG DA FI
3 Sangle longitudinale
NL
N° Sangles Type de fixation
Matériau
Poids
4 Sangles en “V”
ROCK STRAPS 10
Strap
Polypropylène/Nylon 600g
T-STRAPS 10
Strap
Polypropylène/Nylon 800g
REFLEX STRAPS 10
Strap
Polypropylène/Nylon 600g
PIN STRAPS
10
Strap+mousquetons en métal
Polypropylène/Nylon/ Alliage métallique 1500g
ECS STRAPS 12
Strap
Polypropylène/Nylon 800g
RSP STRAPS 10
Strap
Polypropylène/Nylon 350g
NO SV SR
9. MISE EN SERVICE
Pour la première utilisation, vérifier que:
· L’emballage est intègre et qu’il ait protégé le dispositif pendant le transport · Contrôler que toutes les pièces incluses dans la liste d’accompagnement sont présentes. · Fonctionnalités générales du dispositif · État de nettoyage du produit · Absence de déchirures, trous, lacérations ou abrasions sur toute la structure · État d’usure du dispositif. · Vérifier le coulissement correct des sangles · Vérifier le fonctionnement correct des mousquetons s’ils sont présents sur le modèle · Vérifier l’adhésion correcte des inserts de sangles
Vérifier au paragraphe 11 les modalités d’utilisation pour le déroulement des vérifications indiquées ci-dessus. Quelle qu’en soit la raison, ne jamais modifier le dispositif ni ses parties puisque cela pourrait être la cause de dommages aux patients et/ou aux secouristes.
LV ZH JA
25
Le non-respect des mesures indiquées ci-dessus exclut d’utiliser le dispositif en toute sécurité, avec pour conséquence le risque de dommages pour le patient, les
opérateurs ainsi que pour le dispositif.
IT
Pour des utilisations successives, effectuer les opérations spécifiées dans le paragraphe 12. Si les conditions indiquées sont respectées, le dispositif peut être considéré comme prêt à l’emploi; dans le cas contraire, il faut retirer immédiatement le dispositif du service
et contacter le fabricant.
EN
10. CARACTÉRISTIQUES FONCTIONNELLES Pour les caractéristiques de fonctionnement, consulter le paragraphe 11 – Modalités d’utilisation.
DE FR ES PT EL RO CS
11. MODALITÉS D’UTILISATION
Avant d’intervenir sur le patient, des évaluations médicales primaires doivent être effectuées. Avant d’utiliser n’importe quelle typologie de ceinture décrite dans le présent manuel, lire attentivement les instructions d’utilisation du dispositif avec lequel elles doivent être utilisées.
11.1 APPLICATION DES SANGLES
Suivre les procédures approuvées par le service médical d’urgence de référence concernant l’immobilisation, le positionnement et le transport du patient. Les informations citées ci-dessous sont rédigées sur la base d’informations générales d’utilisation. 1. Le patient se trouve placé sur le plan dur avec un collier cervical 2. En maintenant toujours une immobilisation correcte, poser la sangle sur le patient, en mettant les sangles en “V” environ 2/3 cm au-dessous du collier cervical 3. Positionner les autres sangles transversales de cette manière : · la sangle thoracique à la hauteur du thorax juste sous les épaules · la sangle pelvienne à la hauteur des crêtes iliaques · la première sangle des membres inférieurs sur le fémur, près du genou · la deuxième sangle des membres inférieurs sur les tibias, près des chevilles (si le patient est petit, enrouler les sangles)
Faire extrêmement attention aux zones qui peuvent éventuellement avoir subi des traumas et/ou fractures.
4. Appliquer si nécessaire des immobilisateurs de tête et/ou de chevilles. 5. En partant des épaules vers les pieds, introduire les sangles dans les trous correspondants au même moment sur les deux côtés du plan dur en utilisant les mousquetons éventuels qui, si présents, doivent être attachés aux broches du plan dur. 6. Fixer les sangles en appliquant une traction égale sur les deux côtés, des épaules vers les pieds en faisant attention à d’éventuels problèmes respiratoires et abdominaux ; 7. S’assurer que le patient soit correctement immobilisé, continuer les manoeuvres conformément aux lignes directrices du service médical d’urgence de référence.
La sangle pédiatrique RSP, destinée à l’utilisation avec le plan dur pédiatrique Baby Go, est dotée d’un mètre avec des zones colorées, qui permettent d’identifier rapidement le côté susceptible d’être le plus adaptée au patient en fonction de sa taille. Toutefois, le secouriste est le seul responsable du choix du dispositif et de son application correcte.
BG DA FI NL NO SV SR LV ZH JA
12. NETTOYAGE ET ENTRETIEN
Spencer Italia S.r.l. décline toute responsabilité pour tout dommage, direct o indirect, que ce soit comme conséquence d’une utilisation impropre du produit et des pièces détachées et/ou dans tous les cas de n’importe quelle intervention de réparation effectuée par des sujets différents du fabricant, qui utilise des techniciens internes et externes spécialisés et autorisés; de plus, la garantie est invalidée.
· Pendant toutes les opérations de contrôle, d’entretien et de désinfection, l’opérateur doit porter des équipements de protection individuelle appropriés, tels que des gants, des lunettes, etc.
· Établir un programme d’entretien, des contrôles périodiques, et une prorogation du temps de vie moyen, si prévu par le fabricant dans le manuel d’utilisation, en identifiant une personne préposée de référence possédant les exigences de base définies dans le manuel d’utilisation.
· La fréquence des contrôles est déterminée par des facteurs tels que les prescriptions de loi, le type d’utilisation, la fréquence d’utilisation, les conditions environnementales pendant l’utilisation et le stockage.
· La réparation des produits réalisés par Spencer Italia S.r.l. doit être nécessairement effectuée par le fabricant, qui utilise les techniciens internes ou externes spécialisés qui,en utilisant des pièces détachées originales, fournissent un service de réparation de qualitéen conformité étroite avec les caractéristiques techniques indiquées par le producteur. Spencer Italia S.r.l. décline toute responsabilité pour tout dommage, direct ou indirect, qui ce soit la conséquence d’une utilisation impropre des pièces détachées et/ou dans tous les cas, de toute intervention de réparation effectuée par des sujets non autorisés.
· Le reconditionnement, processus exécuté sur le dispositif pour en autoriser la restauration de la sécurité technique et fonctionnelle du dispositif utilisé, comme une nouvelle immatriculation, doit être exécuté par le fabricant.
· Toutes les activités d’entretien et de révision doivent être enregistrées et documentées avec les rapports relatifs d’intervention technique; la documentation devra être conservée au moins pendant 10ans à partir de la fin de vie du produit et devra être mise à disposition des autorités compétentes et/ou du fabricant, si nécessaire.
· Le nettoyage, prévu pour les produits réutilisables, doit être exécuté dans le respect des indications fournies par le fabricant dans le manuel d’utilisation, afin d’éviter le risque d’infections croisées dues à la présence de sécrétions et/ou de résidus.
12.1 NETTOYAGE
La non-exécution des opérations de nettoyage peut entraîner le risque d’infections croisées dues à la présence de sécrétions et/ou de résidus. Pendant toutes les opérations de contrôle et de désinfection, l’opérateur doit porter des équipements de protection individuelle appropriés, tels que des gants, des lunettes, etc.
Les éventuelles pièces métalliques exposées aux agents extérieurs subissent des traitements superficiels et/ou de peinture afin d’obtenir une meilleure résistance. Laver les pièces exposées avec de l’eau tiède et un savon neutre; ne jamais utiliser de solvants ou de détachants. Rincer soigneusement avec de l’eau tiède en vérifiant d’avoir éliminé toute trace de savon, qui pourrait la détériorer ou en compromettre l’intégrité et la durée. Éviter d’utiliser des jets d’eau haute pression. Laisser sécher entièrement avant de la ranger. Le séchage après le lavage ou bien après l’utilisation dans un environnement humide doit être naturel et non forcé: ne jamais utiliser de flamme ou d’autres sources de chaleur directe. Dans le cas d’une désinfection éventuelle, utiliser des produits qui, en plus d’être classés comme des dispositifs médico-chirurgicaux, n’ont pas d’action solvante ou corrosive sur des matériaux constituant le dispositif. S’assurer d’avoir pris toutes les précautions appropriées pour garantir qu’aucun risque d’infection croisée ou de contamination entre patient et opérateur ne subsiste. Dans le cas de produits jetables, aucun nettoyage n’est prévu, sauf si le produit est correctement stocké et emballé comme selon les caractéristiques du fabricant.
12.2 ENTRETIEN ORDINAIRE
Il faut établir un programme de contrôles périodiques, en identifiant une personne de référence. Le sujet auquel est confié l’entretien ordinaire du dispositif doit garantir les exigences de base prévues dans le présent manuel d’utilisation. Toutes les activités d’entretien doivent être enregistrées et documentées avec les rapports correspondants d’intervention technique. Cette documentation devra être conservée au moins pendant 10ans après la fine de vie du dispositif et devra être mise à disposition des autorités compétentes et/ou du fabricant, si nécessaire.
Pendant toutes les opérations de contrôle, d’entretien et de désinfection, l’opérateur doit porter des équipements de protection individuelle appropriés, tels que des gants, des lunettes, etc.
26
Le dispositif ne requiert pas de programme d’entretien ordinaire, mais il faut effectuer des contrôles permettant de vérifier: · Fonctionnalités générales du dispositif · État de nettoyage du dispositif (il faut rappeler que la non-exécution des opérations de nettoyage peut entraîner le risque d’infections croisées) · Satisfaction des exigences prévues par le manuel d’utilisation dans la section 5 Avertissements et 6 Avertissements spécifiques. · Satisfaction des exigences prévues par le manuel d’utilisation dans la section 11Modalités d’utilisation
Utiliser uniquement des composants/pièces détachées et/ou des accessoires originaux ou approuvés par Spencer Italia S.r.l. afin d’effectuer chaque opération sans causer des altérations, des modifications au dispositif; dans le cas contraire, elle décline toute responsabilité sur le fonctionnement incorrect ou sur les éventuels dommages provoqués par le dispositif